Cell重磅|中科院破解尼古丁70年合成之谜:一个糖基化开关,一座液泡超级工厂

肠肝轴代谢 “黄金搭档”:胆汁酸+短链脂肪酸,解码肝病与肠道微生态的核心密码
2026 年 4 月 8 日
中药科研新思路 | 广靶筛尽成分、入血锁定药效,发刊效率拉满
2026 年 4 月 15 日
尼古丁作为烟草中主要的成瘾性和杀虫性生物碱,其生物合成途径的最后步骤困扰了科学界七十余年。近日,中国科学院分子植物科学卓越创新中心李大鹏研究员团队在 Cell 期刊上发表题为“Complete biosynthesis of nicotine”的研究论文。本研究通过信息论指导的多维组学策略,结合无差别串联质谱(idMS/MS)技术,首次完整解析了尼古丁生物合成的全部环节,揭示了一个由糖基化/去糖基化介导的立体选择性分子间Mannich-like缩合反应机制,并发现液泡膜上的五组分代谢体(metabolon)同时负责尼古丁的合成与转运。该研究不仅为理解植物生物碱合成提供了全新范式,更为异源生物合成尼古丁及其在作物抗虫育种中的应用奠定了核心基础。
文章题目:Complete biosynthesis of nicotine
期刊名称:Cell
影响因子:42.5
发表时间:2026年3月
研究团队:中科院分子植物科学卓越创新中心李大鹏团队、德国马普化学生态所
核心突破:整解析尼古丁全生物合成途径,揭示糖基化/去糖基化介导的缩合机制与液泡膜五组分代谢体
研究背景
尼古丁是烟草中兼具强神经毒性、成瘾性与高效杀虫活性的生物碱,也是植物抵御食草动物的核心化学防御武器。1893年尼古丁化学结构被解析,吡咯烷环、吡啶环的来源与上游合成路径早已明确。两大核心问题悬而未决:
a.吡啶环前体烟酸(NA)的真正来源;
b.两个杂环如何缩合形成尼古丁(底物、酶、机制均未知)。
此前研究仅推测A622、BBL蛋白参与缩合,但无法确定NAG(烟酸-N-葡萄糖苷)是合成前体还是解毒副产物,导致完整通路始终无法闭合。解析这一“最后一步”,成为植物次生代谢领域最关键的科学难题之一。
主要结论
1.隐秘的糖基化/去糖基化机制
尼古丁并非直接缩合生成,而是通过糖基化激活→还原→立体缩合→氧化→去糖基化的级联反应完成,糖基化是必需的活化步骤。
2.全新烟酸供给途径
吡啶环支路中,烟酸(NA)由NaNAMNH直接水解NAMN生成,完全不依赖NAD循环,是烟草特化的尼古丁专用合成支路。
3.液泡膜五组分代谢通道体
NaUGT1、NaA622、NaBBL2、NaBGL1 与转运蛋白NaMATE1在液泡膜动态组装,实现底物通道化、手性控制、合成-转运一体化,避免有毒中间体泄露。
4.跨物种异源合成与抗虫应用
在番茄、茄子、豌豆中成功重构尼古丁合成通路,NaMATE1是高效合成的关键;转基因豌豆可高水平合成尼古丁,显著提升抗虫能力。
研究结果
1.多维组学策略精准捕获尼古丁生物合成的时空变异
研究团队构建模拟昆虫取食诱导系统(W+OS),利用乙烯信号突变体(irACO、sETR1)与碳分配调控株系(asGAL83),结合时序转录组、代谢组、mQTL、单细胞测序,系统锁定尼古丁合成核心基因模块。
•信息论指导的代谢组解析:计算代谢多样性指数(Hj)与特化指数(δj),发现irACO与sETR1株系诱导后代谢特化显著增强,尼古丁大量积累;
•时序共表达分析:NaODC、NaPMT1/2、NaMPO、NaAO2、NaQS、NaQPT1/2、NaA622、NaBBL2等基因在诱导后5–17小时高度协同上调;
•mQTL定位:对643个MAGIC重组自交系分析,除已知合成基因外,首次定位到NaUGT1(5号染色体)与NaBGL3/4(10号染色体),直接指向糖基化与去糖基化步骤;
•单细胞转录组:MeJA诱导后,NaUGT1、NaBGLs、NaBBLs与尼古丁合成基因在根皮层、内皮层、根冠细胞特异性共表达;
•多维共关联网络:所有尼古丁合成基因形成紧密核心簇,NaUGT1、NaBGLs位于网络中心,证明糖基化/去糖基化是缩合反应的核心环节。
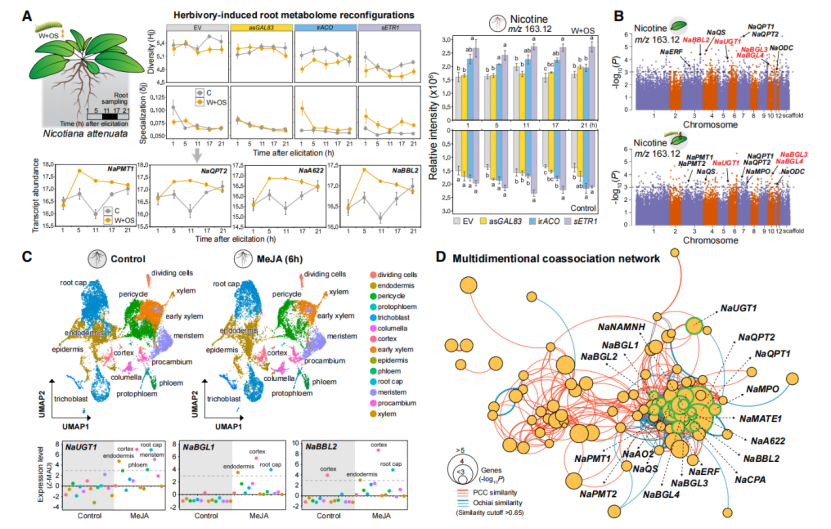
图1 多维组学揭示尼古丁合成的时空同步基因模块
2.尼古丁缺失突变体揭示不依赖NAD循环的全新吡啶合成支路
团队在转基因株筛选中意外获得一株完全不产尼古丁、但表型正常的突变体ao2,成为破解吡啶前体来源的关键。
•突变基因为NaAO2,第一外显子C→T突变导致蛋白提前终止,MeJA诱导后尼古丁含量下降超100倍;
•回补NaAO2可完全恢复尼古丁合成;
•外源饲喂烟酸(NA)或烟酰胺(NAM),可完全恢复尼古丁积累;
•结合idMS/MS无偏向代谢组,鉴定出NaNAMNH(NAMN水解酶),体外酶活证实其直接催化NAMN→烟酸(NA);
•VIGS沉默与CRISPR敲除NaNAMNH,尼古丁含量显著下降;
最终证明:尼古丁吡啶前体由NAMN直接水解而来,完全不依赖NAD循环,是烟草进化出的专用支路。
3.糖基化中间体是尼古丁合成的核心激活底物
通过信息论与结构代谢组分析,在ao2突变体饲喂NA后,特异性富集到3个关键糖苷中间体,并用标准品逐一验证结构:
1.NAG(烟酸-N-葡萄糖苷,m/z 286.09)
2.PG(吡啶-N-葡萄糖苷,m/z 242.10)
3.NG(尼古丁-N-葡萄糖苷,m/z 325.18)
三者均丢失162.05Da葡萄糖中性丢失,证明糖基化是尼古丁合成的必需激活步骤,推翻过去“NAG只是解毒产物”的错误认知。
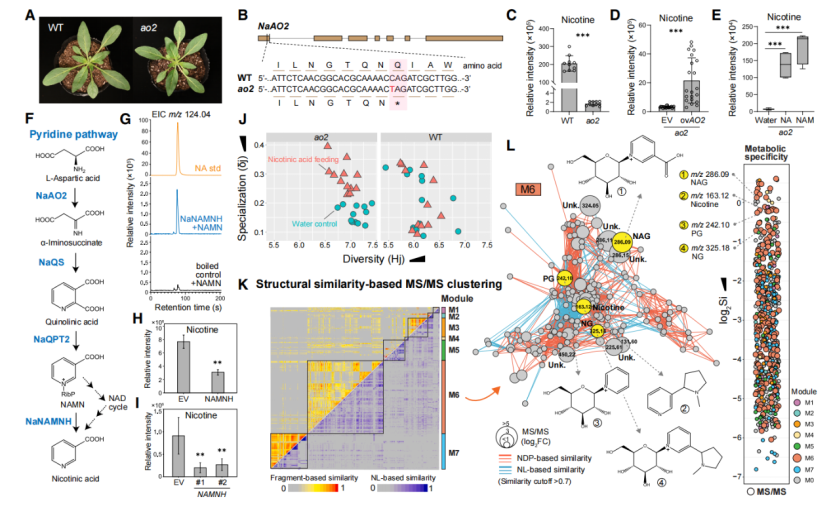
图2 无尼古丁突变体与代谢组揭示NAMN水解酶及糖基化中间体参与尼古丁合成
4.完整尼古丁生物合成途径的体外与体内重构验证
基于以上发现,团队提出并严格验证了完整尼古丁生物合成路线:
1. 烟酸(NA)→NaUGT1→NAG(糖基化激活)
2.NAG→NaA622→还原脱羧→二氢吡啶-N-葡萄糖苷
3.二氢吡啶-N-葡萄糖苷+MP→立体选择性Mannich-like缩合
4.缩合产物→NaBBL1/2→氧化→NG(尼古丁-N-葡萄糖苷)
5.NG→NaBGL1/2→尼古丁(去糖基化释放)
多重体系验证:
•本氏烟瞬时表达:共表达全套基因可高效合成D3-尼古丁;缺失NaA622积累NAG,缺失NaBBL2积累二氢尼古丁糖苷,缺失NaBGL1积累NG;
•酵母异源重构:以鸟氨酸与D4-NA为底物,成功实现从头合成尼古丁;
•体外酶活:NaUGT1催化NA→NAG,NaA622催化NAG+MP→NG,NaBGL1/2催化NG→尼古丁;
•植物体内验证:
○VIGS沉默NaUGT1或NaBGL1/2→尼古丁显著下降;
○CRISPR敲除A622、UGT1→尼古丁完全消失;
○MATE1突变体→尼古丁降至野生型2/3;
○irBBL RNAi株系→尼古丁诱导完全受阻。
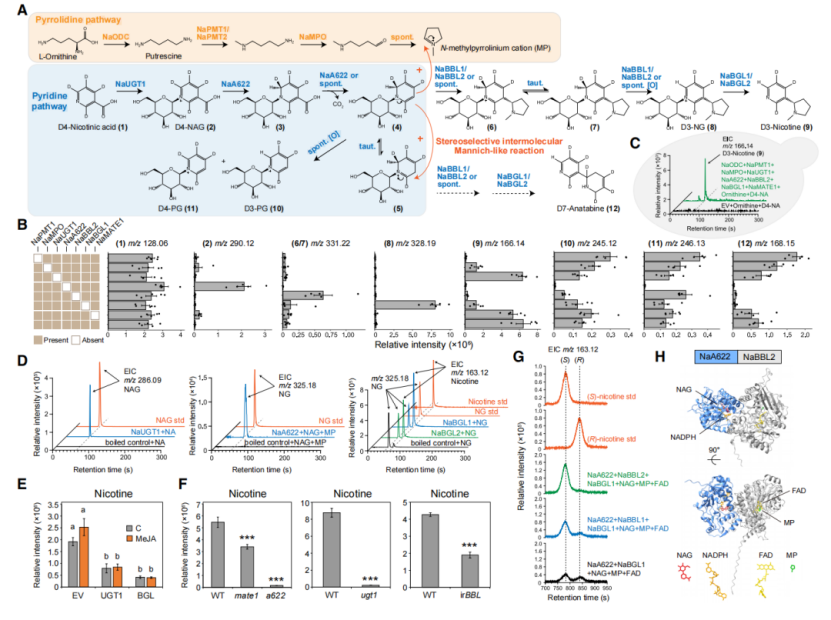
图3 尼古丁合成通路在体外与异源体系中的重构与功能验证
5.NaBBL1/2控制尼古丁立体选择性,专一产(S)-尼古丁
手性是尼古丁生物活性的关键,植物只产(S)-尼古丁。
•体外仅NaA622+NaBGL1→产生等量S/R尼古丁;
•加入NaBBL1/2→几乎专一产生(S)-尼古丁;
•AlphaFold3建模显示:NaA622结合NADPH与NAG,NaBBL2结合FAD与MP,两者形成紧密酶-酶界面;
•界面氨基酸突变→蛋白互作减弱→尼古丁产量大幅下降。
6.液泡膜五组分动态代谢体:合成+转运一体化超级工厂
所有关键蛋白均定位于液泡膜,并组装成五组分动态代谢体:
•成员:NaUGT1、NaA622、NaBBL2、NaBGL1、NaMATE1
•多重互作证据:BiFC、Split-LUC、FLIM-FRET、Pull-down、MST(Kd达nM级)
•底物通道化实验:先期饲喂D4-NA,再加入未标记NAG,不改变D3-尼古丁同位素丰度,证明中间体完全在复合体内通道化传递,不泄露到细胞质;
•核心功能:
a.隔离有毒中间体,避免植物自毒;
b.保证立体选择性,只产(S)-尼古丁;
c.合成-转运同步完成,直接存入液泡。
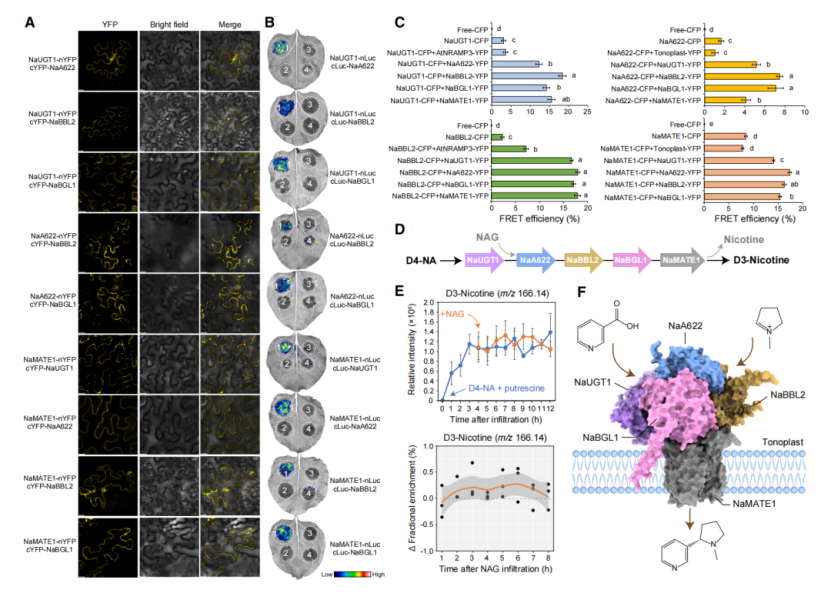
图4 液泡膜上多酶复合体形成代谢区室,介导尼古丁合成与转运的通道化过程
7.跨作物异源重构,赋予植物强抗虫性
团队在番茄、茄子、豌豆中重构完整尼古丁合成与转运通路:
•所有作物均可高效合成尼古丁;
•NaMATE1是异源高效合成的必需因子,缺失则产量骤降;
•豌豆重构株尼古丁含量接近烟草水平;
•抗虫测试:斜纹夜蛾取食转基因豌豆叶片
○幼虫体重仅为对照1/2
○死亡率:39.3%→60.7%
证明该通路可直接用于作物绿色抗虫育种。
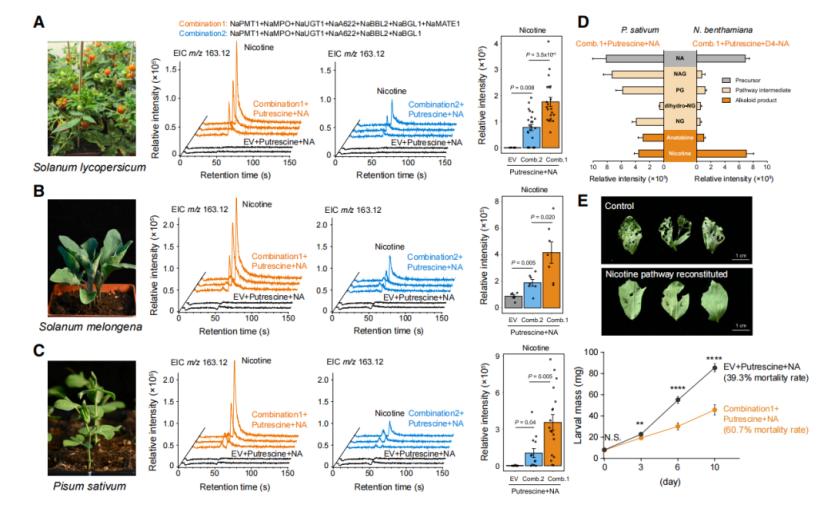
图5 尼古丁合成代谢区室在异源植物中重构并增强抗虫性
文章总结
本研究以多维组学为核心方法,完成从基因挖掘→中间体鉴定→通路解析→机制阐明→应用转化的全链条突破,首次完整解析尼古丁生物合成全通路,揭示植物通过糖基化屏蔽+代谢区室高效合成复杂生物碱的通用策略,为生物碱合成生物学、低害烟草育种、绿色抗虫作物培育提供核心基因资源与全新理论范式。
植物广靶定量代谢组技术
广靶定量代谢组学,结合了“非靶向代谢组学”的“广覆盖”(测得多)和“靶向代谢组学”的“准定量”(测得准)的优势,一次检测就能同时完成植物70000+种代谢物的定性和准确定量,涵盖糖、氨基酸、黄酮、萜类、生物碱、激素等关键物质 ,通过稳定同位素内标与基质匹配校正,实现精准定量(单位:ug/mL)。单次可以高通量定性定量检出超过3000+种代谢物,能够挖掘更丰富、更精准、更有效的代谢组学数据,助力科研新发现。
产品优势:
高精准定量分析:多标线性定量,提供代谢物浓度信息(ug/mL);
双平台检测:高分辨质谱仪器+低分辨质谱仪器对代谢物进行检测,同时兼顾定性和定量准确;
超高通量:一次性靶向检测自建数据库中70000多种代谢物,包括物种特有的代谢物,全覆盖糖类、醇类、氨基酸、有机酸、核苷酸、脂质、维生素、苯丙素类、黄酮类、生物碱类、萜类、甾体等多种类型的代谢物;
高灵敏度:低丰度物质检出效果好,最低实现pg级物质检测;
精准定量:MRM多反应监测模式是定量“金标准”;
检出领先:根、茎、叶、花等组织中可检出3000+种代谢物,更全面表征样本代谢谱;
检测稳定:7大质控,层层把关,提供优质数据;
分析智能:自动识别信号峰,兼具准确与高效,尤适合于大规模样本研究;
深度挖掘:采用云平台交付,提供多组学关联,助力数据挖掘。



