开年大捷!NC案例+1!中国农业大学马云飞团队深度解析神经肽SP同步破解结肠炎与焦虑的关键机制

突破・精准・全覆盖 | 高精准量化,赋能脂质组学深度研究
2026 年 1 月 29 日
项目文章 | 帕金森病治疗添新招!广州医科大学团队揭秘RRx-001的“中枢+肠脑轴”调控机制
2026 年 2 月 11 日
炎症性肠病(IBD)与焦虑、抑郁的“共病困境”长期困扰临床——高达30%的IBD患者伴随焦虑症状,而情绪障碍又会反向加重肠道炎症,形成难以打破的恶性循环。长期以来,临床治疗多“分而治之”,缺乏同时靶向肠道炎症与精神症状的整合性方案。
近日,中国农业大学团队在Nature Communications(IF=15.7)发表的重磅研究,为这一难题提供了全新解决方案:神经肽SP(Substance P)可通过重塑肠道菌群、促进菌群代谢物肌醇生成,同步改善DSS诱导的结肠炎与焦虑样行为。这项研究不仅阐明了“SP-肠道菌群-肌醇-海马体信号通路”的完整调控链,更以多组学技术与严谨的动物实验验证其机制,为IBD合并精神障碍的治疗开辟了新赛道。
百谱生物为该研究提供了非靶代谢组检测服务!

文章题目:Neuropeptide SP protects against colitis and linked anxiety-like behavior through the putative roles of gut microbiota and metabolite inositol
中文题目:神经肽SP通过肠道微生物群和代谢物肌醇的假定作用保护机体免受结肠炎及相关焦虑样行为的影响
期刊名称:Nature Communications
影响因子:15.7
发表单位:中国农业大学兽医学院等
研究方法:非靶代谢组学、微生物组和转录组等

1. 临床痛点:IBD与精神症状的恶性循环
IBD是一种慢性非特异性肠道炎症,包括溃疡性结肠炎和克罗恩病,患者除了腹泻、便血、肠黏膜损伤等肠道症状,还常面临焦虑、抑郁等精神困扰。临床数据显示,IBD患者焦虑发生率达30%,抑郁发生率达25%,这些精神症状不仅严重降低患者生活质量,还会通过“脑-肠轴”加剧肠道炎症,导致疾病反复发作、难以根治。
2. 科学缺口:肠脑轴调控的黑箱待解
菌群-肠-脑轴(MGB轴)是连接肠道与大脑的核心通路——肠道菌群通过代谢物、炎症因子等信号分子,与中枢神经系统实现双向沟通。已有研究证实,IBD患者的肠道菌群失衡会破坏肠道屏障完整性,让炎症因子进入血液循环,进而诱发海马体神经炎症,干扰神经递质平衡,最终导致焦虑样行为。
3. 研究目标:破解SP的双向保护机制
- SP是否能同时改善IBD相关肠道炎症与焦虑样行为?
- 肠道菌群是否为SP发挥作用的必需媒介?
- SP调控肠脑轴的关键代谢物与脑内信号通路是什么?


实验设计:采用4%DSS饮水诱导小鼠溃疡性结肠炎模型,通过静脉注射SP干预,从“肠道病理-肠道屏障-炎症因子-行为学” 多维度验证SP的保护作用。
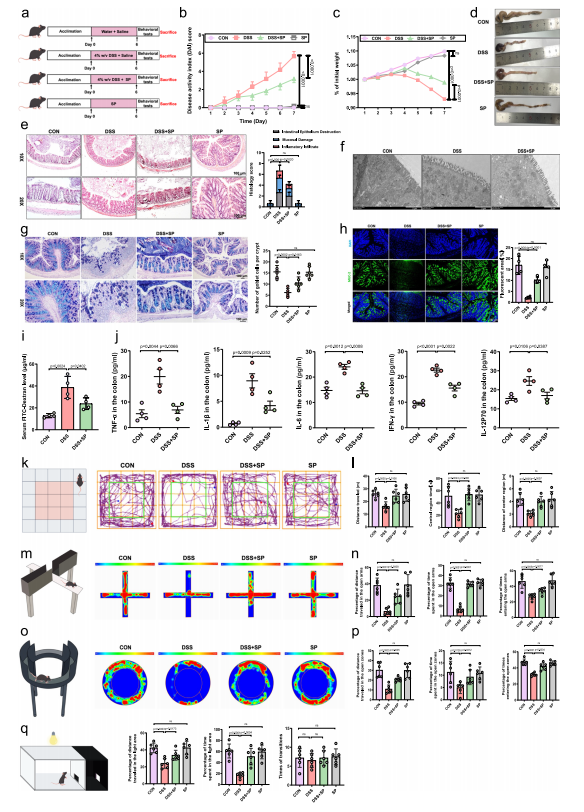
图1 SP改善DSS诱导小鼠的结肠炎症状及焦虑样行为
- 肠道层面:SP显著缓解DSS诱导的体重下降、直肠出血、结肠缩短,降低DAI评分;保护肠黏膜完整性,减少炎症浸润与隐窝损伤,修复肠道超微结构,上调MUC-2表达、增加杯状细胞数量,降低肠道通透性,减少TNF-α、IL-1β等促炎因子释放。
- 行为学层面:经OFT、EPM、EZM、LDB四大焦虑模型验证,SP可逆转DSS诱导的焦虑样行为,提升小鼠对开放区域的探索,减少对黑暗/封闭环境的回避。
DSS撤药后肠道炎症消退,SP仍能改善残留焦虑样行为,表明其对肠脑轴的调控不依赖肠道炎症缓解,具有独立性。

实验设计:IBD相关神经炎症会导致海马体神经元损伤、神经递质失衡。通过组织学染色、细胞标记与细胞因子检测,探究SP对海马体的保护作用。
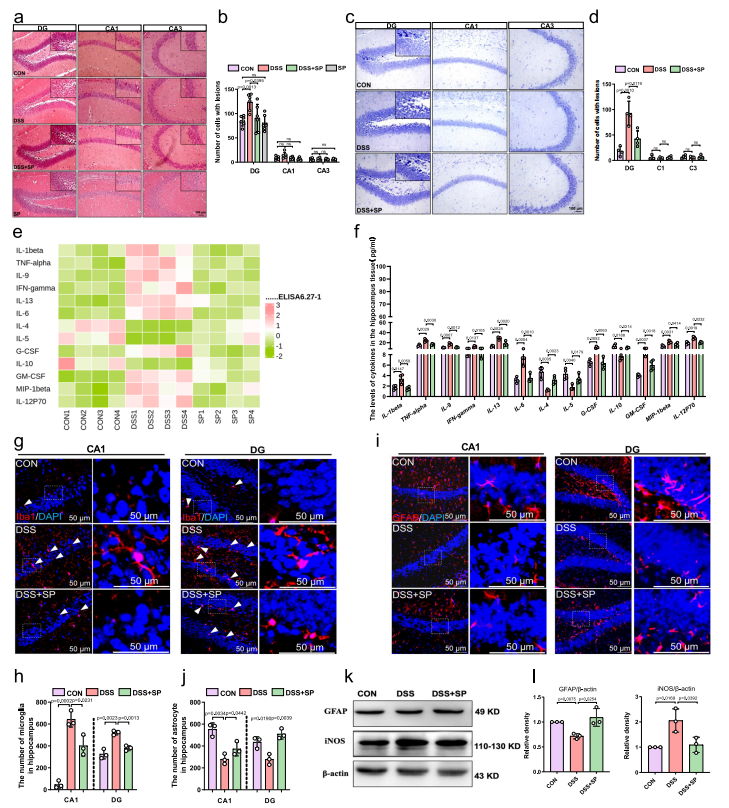
图2 SP减轻DSS诱导小鼠的海马损伤及神经炎症反应
- 形态保护:SP显著减轻DSS诱导的海马体神经元丢失、核固缩、尼氏小体减少等病理损伤,维持神经元形态完整。
- 炎症调控:SP显著降低海马体中IL-1β、TNF-α、IL-6等促炎因子水平,同时上调IL-4、IL-5、IL-10等抗炎因子表达,重构神经炎症平衡。
- 细胞保护:抑制小胶质细胞激活与M1表型极化,逆转星形胶质细胞丢失,二者功能修复是SP抗焦虑的关键细胞基础。
明确SP的神经保护靶点为海马体,且与调控小胶质细胞、星形胶质细胞功能密切相关。

实验设计:探究SP是否通过肠道菌群发挥作用,通过16SrRNA测序分析SP对DSS诱导菌群失调的调控作用,结合PICRUSt2预测菌群代谢功能。
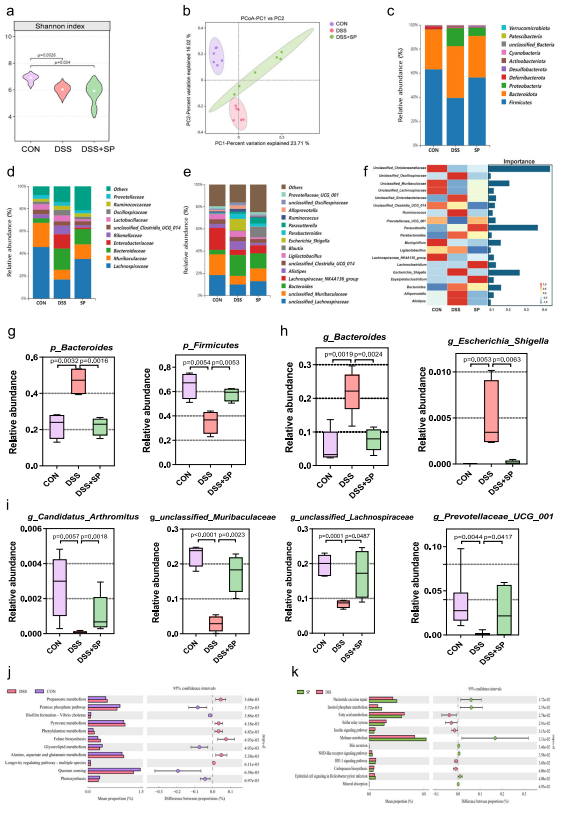
图3 SP改善DSS诱导小鼠肠道菌群失调并改变微生物组功能
- 菌群结构重塑:SP对肠道菌群α多样性无显著影响,但显著改变β多样性,使DSS紊乱的菌群结构向正常组趋近。
PICRUSt2预测显示,SP激活肌醇磷酸代谢、胆汁分泌、NOD样受体信号通路等有益功能模块,抑制生物膜形成、群体感应等致病相关通路。

实验设计:采用“抗生素鸡尾酒”(氨苄西林+甲硝唑+万古霉素+新霉素+庆大霉素)处理14天,耗竭小鼠肠道菌群,验证肠道菌群是否为SP发挥作用的必需环节。
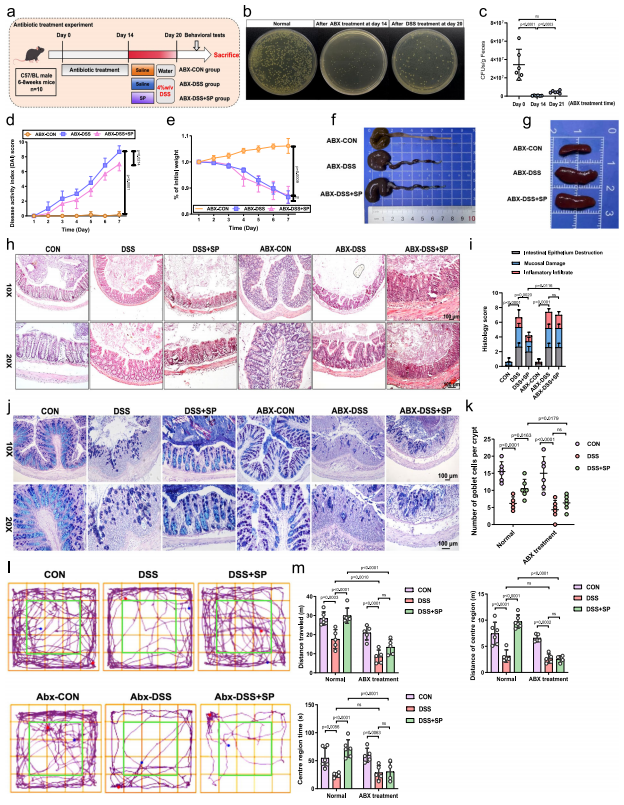
图4 SP以肠道微生物群依赖性方式预防DSS诱导的肠道损伤及焦虑样障碍
- 菌群耗竭成功:抗生素处理后,小鼠粪便细菌菌落数显著降低,粪便DNA含量减少,盲肠显著肿大,证实肠道菌群被有效耗竭。
- SP保护作用失效:菌群耗竭后,SP对DSS诱导的结肠炎及焦虑样行为的改善作用完全消失,肠道屏障通透性与炎症因子水平未得到有效调控。
直接证实SP的保护作用依赖肠道菌群,排除SP直接穿过血脑屏障发挥作用的可能,明确菌群是SP调控肠脑轴的核心“中间人”。

实验设计:将SP处理后的小鼠粪便移植给DSS诱导的结肠炎小鼠,验证菌群是否能直接传递SP的双向保护作用。
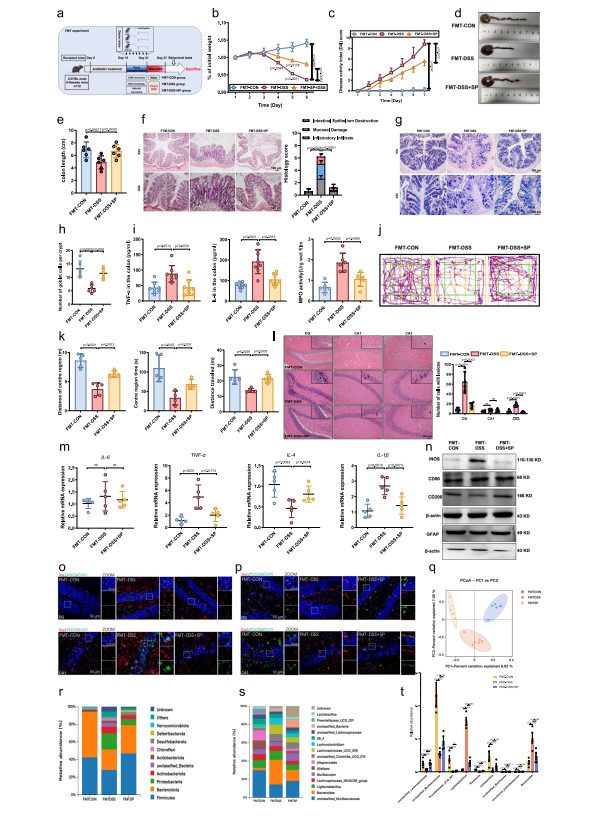
图5 FMT实验表明,SP通过调节肠道菌群减轻了DSS诱导的结肠炎和焦虑样行为
- 肠道保护传递:FMT-DSS+SP组结肠炎症状显著缓解,体重恢复、结肠长度增加,肠黏膜损伤与促炎因子水平降低,黏液屏障功能恢复。
- 神经保护传递:小鼠焦虑样行为改善,海马体神经元损伤减轻,小胶质细胞M1表型比例降低、M2表型比例升高,星形胶质细胞丢失逆转。
- 菌群重构验证:16S rRNA测序显示,FMT-DSS+SP组菌群结构与SP处理组一致,抗炎菌丰度升高、促炎菌丰度降低。
明确SP调控的肠道菌群是其保护作用的“功能载体”,为后续筛选关键功能菌群与代谢物奠定基础。

实验设计:通过转录组测序分析FMT处理小鼠海马体的差异表达基因,结合WB、免疫荧光染色,明确SP调控菌群后对脑内信号通路的影响。
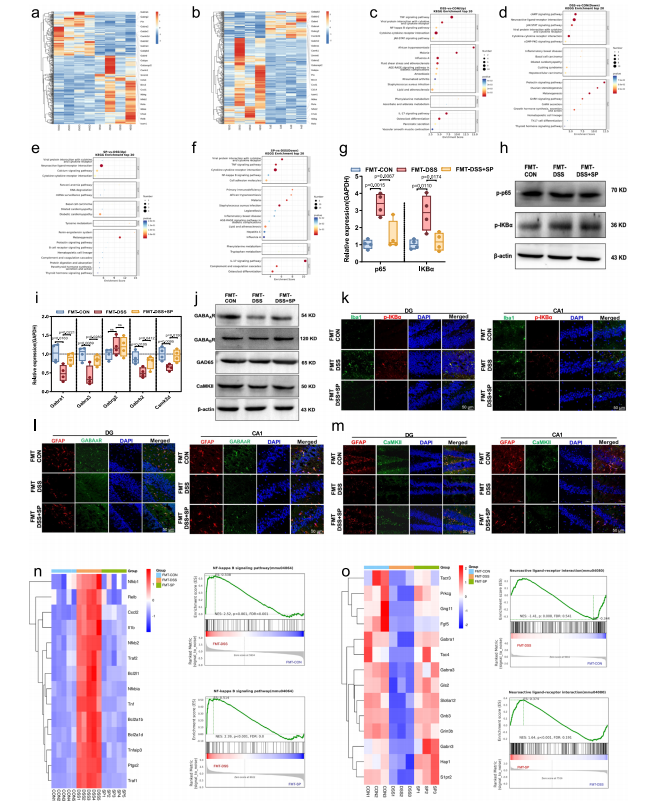
图6 SP通过调节肠道微生物组影响海马基因的表达
- 抑制NF-κB通路:FMT-DSS+SP组显著抑制海马体NF-κB激活,减少小胶质细胞促炎反应。
- 激活GABAergic/Ca²⁺抗焦虑通路:上调GABA受体、CaMK2d等基因与蛋白表达,激活抗焦虑信号。
- 细胞特异性验证:SP调控的菌群可靶向抑制小胶质细胞促炎基因,激活星形胶质细胞GABA能相关基因。

实验设计:肠道菌群通过代谢物介导肠脑轴沟通,采用非靶向代谢组学分析DSS、DSS+SP、CON三组小鼠的结肠内容物代谢谱,筛选SP调控的关键代谢物。
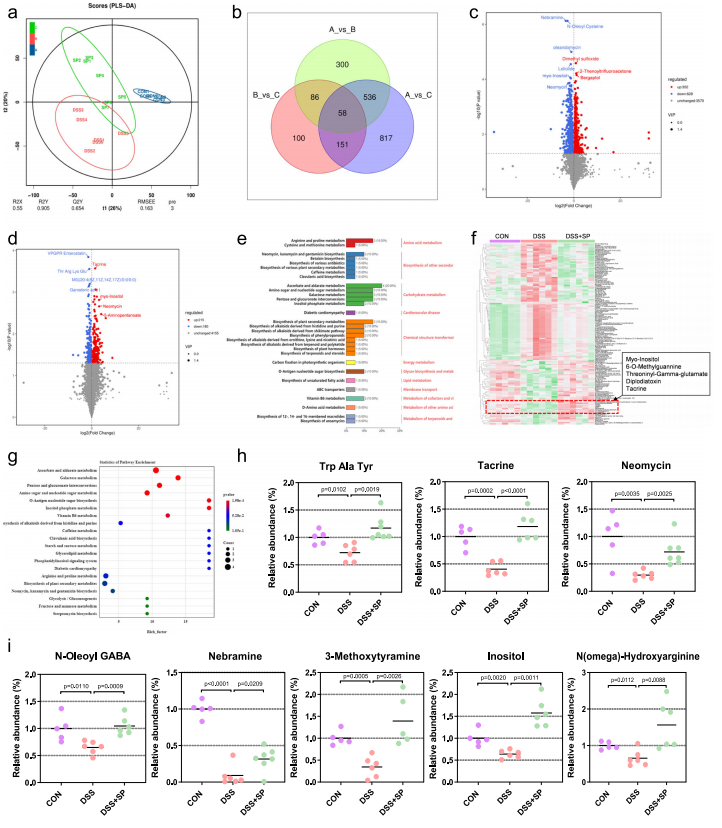
图7 SP可增强肠道微生物群源代谢物肌醇的富集
- 代谢谱分离:PLS-DA分析显示,三组代谢谱存在显著分离,DSS+SP组代谢表型更接近CON 组,表明SP可逆转 DSS 诱导的代谢紊乱。
- 关键代谢物筛选:共鉴定出395个差异代谢物,其中肌醇(inositol)是SP干预后升高最显著的代谢物之一,且富集于肌醇磷酸代谢、半乳糖代谢等通路。
Spearman相关性分析显示,肌醇水平与有益菌群呈正相关,与结肠炎严重程度呈负相关,提示肌醇可能是菌群介导 SP 保护作用的关键 “信使分子”。

实验设计:通过饮水给予DSS诱导的结肠炎小鼠2%肌醇干预,验证肌醇是否能单独模拟SP的双向保护作用。

图8 肠道代谢物肌醇介导SP对DSS诱导小鼠结肠炎及焦虑行为的保护作用
- 肠道保护:缓解DSS诱导的体重下降、DAI升高、结肠缩短,修复肠黏膜,上调E-cadherin,降低结肠促炎因子水平。
- 神经保护:改善焦虑样行为,减轻海马体损伤与神经炎症,降低小胶质细胞激活;促进GABA合成与受体表达,增加星形胶质细胞及GAT1免疫阳性表达。
安全性验证:肌醇单独处理组与正常对照组无显著差异,表明其无明显毒性。

实验设计:采用肌醇合成抑制剂L-690330干预,验证肌醇是否为SP发挥作用的必需分子;同时通过体外细胞实验,验证肌醇对小胶质细胞与星形胶质细胞的直接调控作用。
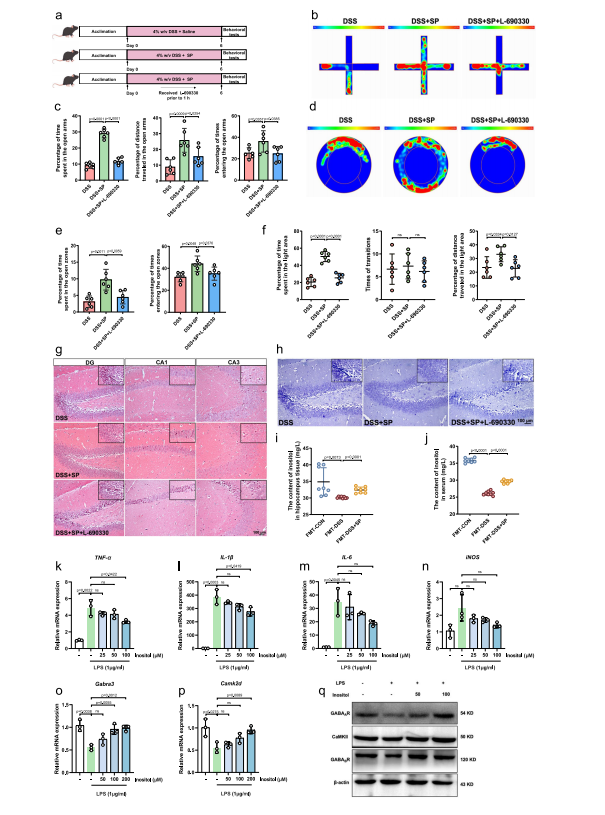
图9 胞内酰胺在SP对DSS诱导小鼠焦虑样行为的作用中发挥关键作用
- 逆转SP的保护作用:L-690330处理后,SP对DSS小鼠的抗焦虑作用及海马体保护效应被显著逆转。
- 肌醇水平升高:FMT-DSS+SP组小鼠海马体与血清中肌醇浓度显著高于FMT-DSS组,证实菌群衍生的肌醇可进入血液循环并作用于大脑。
- 体外细胞验证:
① 小胶质细胞(BV-2):100μM肌醇可显著降低LPS诱导的TNF-α、IL-1β、IL-6 等促炎因子表达,无细胞毒性;
② 星形胶质细胞(C8D1A):肌醇可逆转LPS诱导的GABA受体及CaMKII蛋白表达下调,激活GABAergic/Ca²⁺信号通路。
明确肌醇在SP调控通路中的“不可替代”地位,同时证实肌醇可直接调控神经细胞功能,完善“菌群代谢物 – 脑”的调控链条。

核心逻辑总结:SP通过调节肠道菌群结构,促进有益菌群产生肌醇;肌醇进入循环后作用于海马体,一方面抑制小胶质细胞NF-κB促炎通路,减轻神经炎症;另一方面激活星形胶质细胞 GABAergic/Ca²⁺信号通路,增强抗焦虑神经传导;最终实现对结肠炎的肠道保护与焦虑样行为的神经调节,形成“SP-肠道菌群-肌醇-海马体”的完整调控轴。
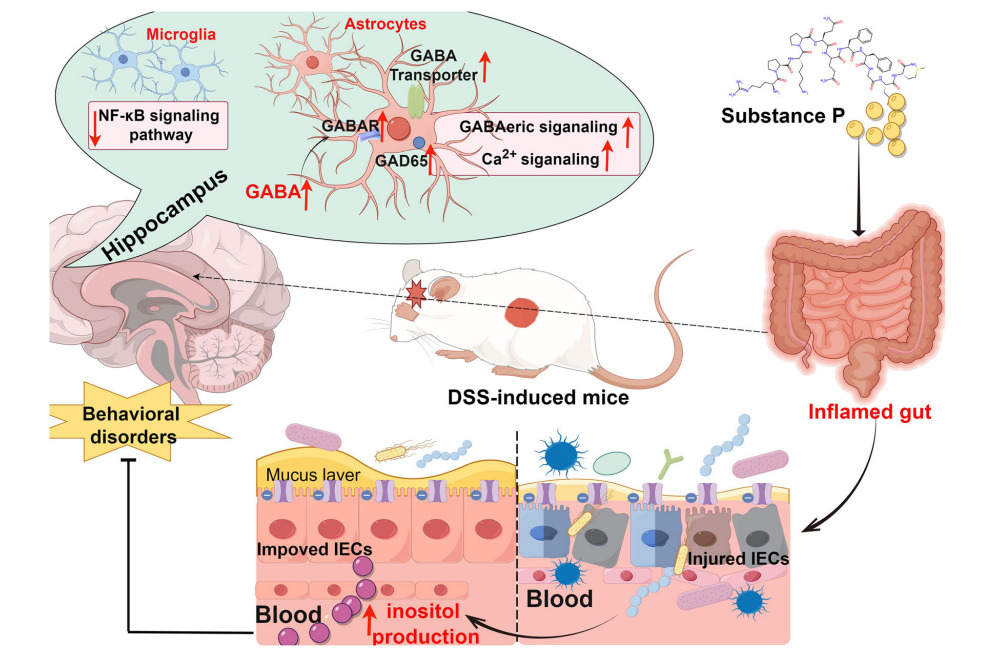
图10 示意图阐释了SP预防结肠炎及焦虑样行为的作用机制





