抗PD-1疗效差、易耐药?南京医科大学新研究:竟是它在抑制免疫杀伤

Food Chemistry | 青海大学和安徽农业大学联合解析牦牛-西门塔尔牛瘤胃菌群调控乳汁营养的核心机制
2026 年 3 月 23 日
盐碱逆境求生记:转录组与代谢组揭示玉米通过ZmWRKY82调控黄酮合成实现ROS清除与耐逆升级
2026 年 3 月 31 日
肺腺癌免疫治疗中,免疫检查点抑制剂响应率低、易耐药的问题亟待解决,“冷肿瘤” 导致的CD8⁺T细胞浸润不足是核心瓶颈,传统研究多聚焦肿瘤细胞,却忽视了癌相关成纤维细胞的关键调控作用。
近日,江苏省肿瘤医院团队在Cell Death & Disease(IF=9.6)发表研究,首次揭示FAP⁺癌相关成纤维细胞高表达LINC01711构建乳酸免疫抑制屏障的机制,并研发出sEV介导的siRNA递送系统靶向敲低该基因,可有效恢复CD8⁺T细胞功能,显著提升肺腺癌抗PD-1治疗效果,为免疫治疗增敏提供全新策略。
百谱生物为该研究提供了代谢组检测服务!

文章题目:Targeting LINC01711 in FAP⁺ cancer-associated fibroblasts overcomes lactate-mediated immunosuppression and enhances anti-PD-1 efficacy in lung adenocarcinoma
期刊名称:Cell Death & Disease
影响因子:9.6
研究方法:荧光原位杂交与免疫荧光染色、体外激酶实验、Western blotting、 pull-down、RIP、BiFC、IP/Co-IP、RNA-seq及非靶向代谢组等
发表单位:南京医科大学、江苏省肿瘤医院等
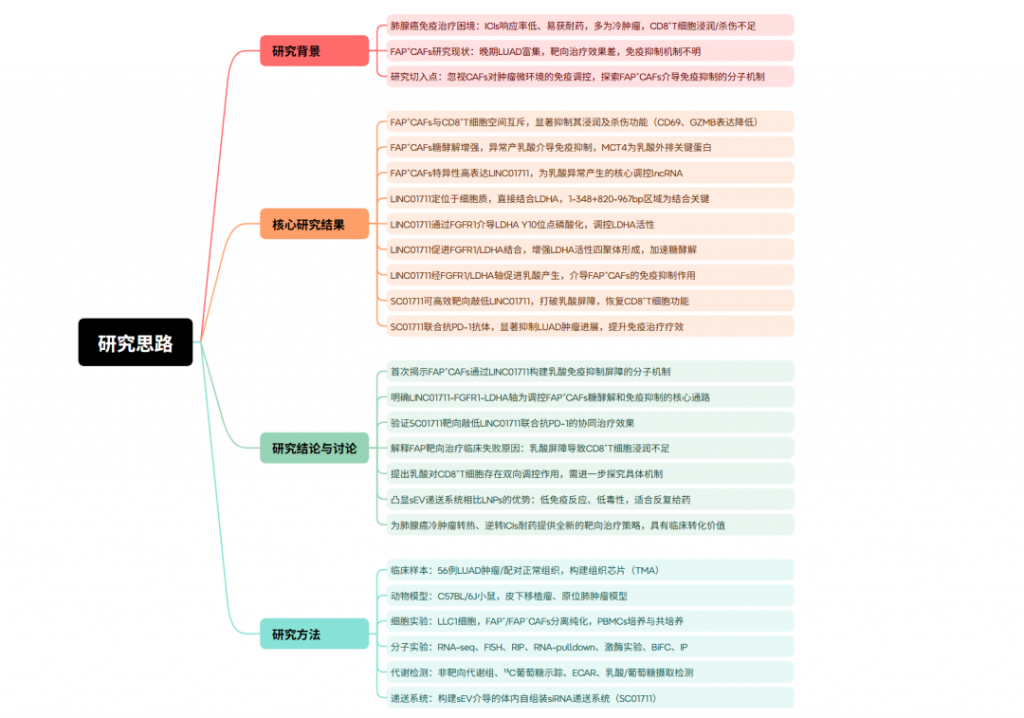
研究背景
PD-1单抗联合化疗可改善晚期非小细胞肺癌一线治疗效果,但免疫检查点抑制剂应答率低、易出现获得性耐药,这与多数肿瘤为“冷肿瘤”、T细胞浸润不足密切相关。癌症相关成纤维细胞是肿瘤微环境主要细胞,具有异质性,其中成纤维细胞活化蛋白阳性亚型在晚期肺癌中占主导,还可抑制T细胞功能,但相关靶向治疗效果不佳。因此,深入探究FAP⁺ CAFs介导肺癌免疫耐受的分子机制,开发有效治疗策略,对提高免疫治疗应答率具有重要意义。
研究材料
组织样本:本研究纳入2016-2020年南京医科大学附属肿瘤医院(江苏省肿瘤医院)56例肺腺癌患者的肿瘤组织及配对正常肺组织样本,所有样本均由两名资深病理医师确诊。收集新鲜样本并制作石蜡包埋组织芯片,所有患者均具备完整的临床资料和随访数据。
转录组测序:收集癌症相关成纤维细胞
非靶向代谢组学分析:收集癌症相关成纤维细胞
研究结果
01 FAP⁺CAFs 保护肺腺癌细胞免受细胞毒性T淋巴细胞的杀伤
为探究肺腺癌中成纤维细胞活化蛋白阳性癌症相关成纤维细胞与免疫浸润的关系,作者通过癌症基因组图谱-肺腺癌数据库和TIMER数据库分析发现,成纤维细胞活化蛋白高表达与细胞毒性T淋巴细胞浸润减少、癌症相关成纤维细胞浸润增加显著相关,且该阳性亚型高浸润患者总生存期更短,结合细胞毒性T淋巴细胞浸润情况后差异更显著。对56例肺腺癌组织芯片的免疫荧光分析,验证了生存结果,并观察到二者存在空间排斥现象且丰度呈负相关。进一步体内外实验显示,与成纤维细胞活化蛋白阴性亚型相比,阳性亚型可显著减少细胞毒性T淋巴细胞浸润、降低其细胞毒性(CD69和GZMB表达下调),且体内实验中会加速肿瘤进展。
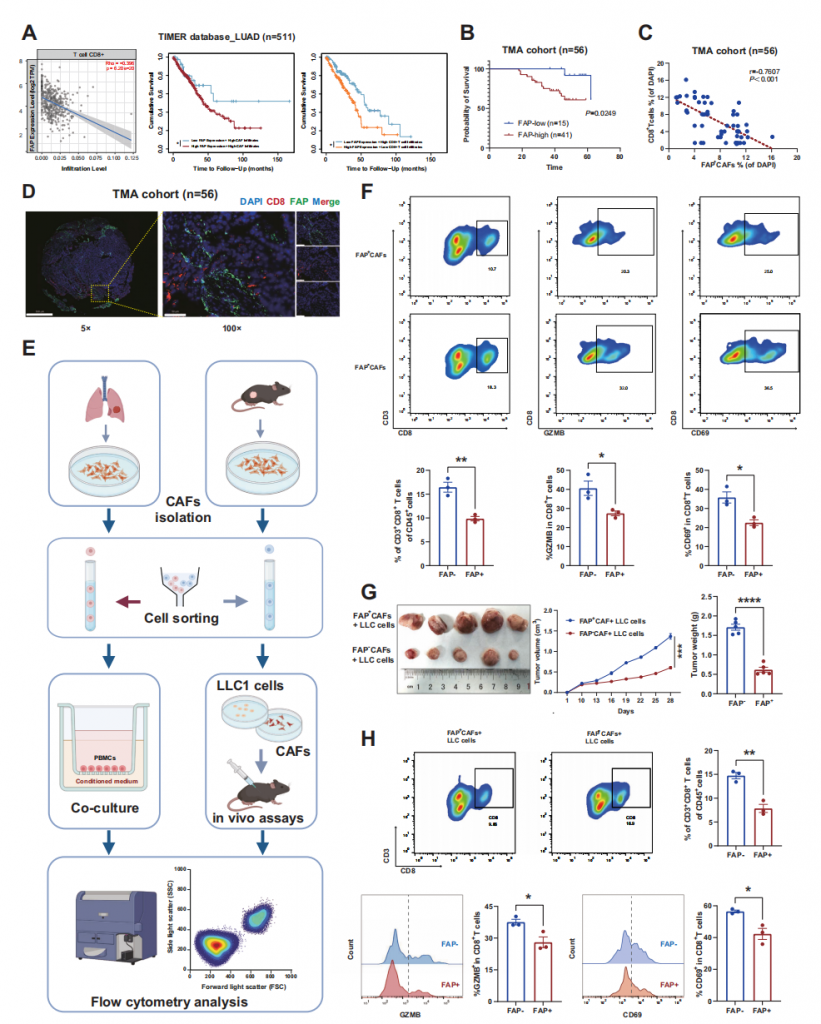
图1 FAP⁺ CAFs保护LUAD肿瘤细胞免受CD8⁺T细胞攻击
02 FAP⁺CAFs对细胞毒性T淋巴细胞的抑制作用依赖于其异常的乳酸生成
作者进一步探究成纤维细胞活化蛋白阳性癌症相关成纤维细胞调控免疫浸润的机制,发现其培养基较阴性亚群更快变黄,且TGF-β和IL-10表达无显著差异,推测其有氧糖酵解效率增强。非靶向代谢组学、细胞外酸化率等实验证实,该阳性亚型糖酵解相关代谢产物浓度、糖酵解效率及乳酸生成均显著高于阴性亚群。调控实验显示,体外加入外源性乳酸可降低细胞毒性T淋巴细胞浸润和毒性,加入乳酸受体抑制剂3-羟基丁酸则可恢复;体内实验也验证了这一结论,乳酸会加速肿瘤进展、抑制免疫,3-羟基丁酸则可逆转该效应,证实阳性亚型对细胞毒性T淋巴细胞的抑制作用依赖异常乳酸生成。
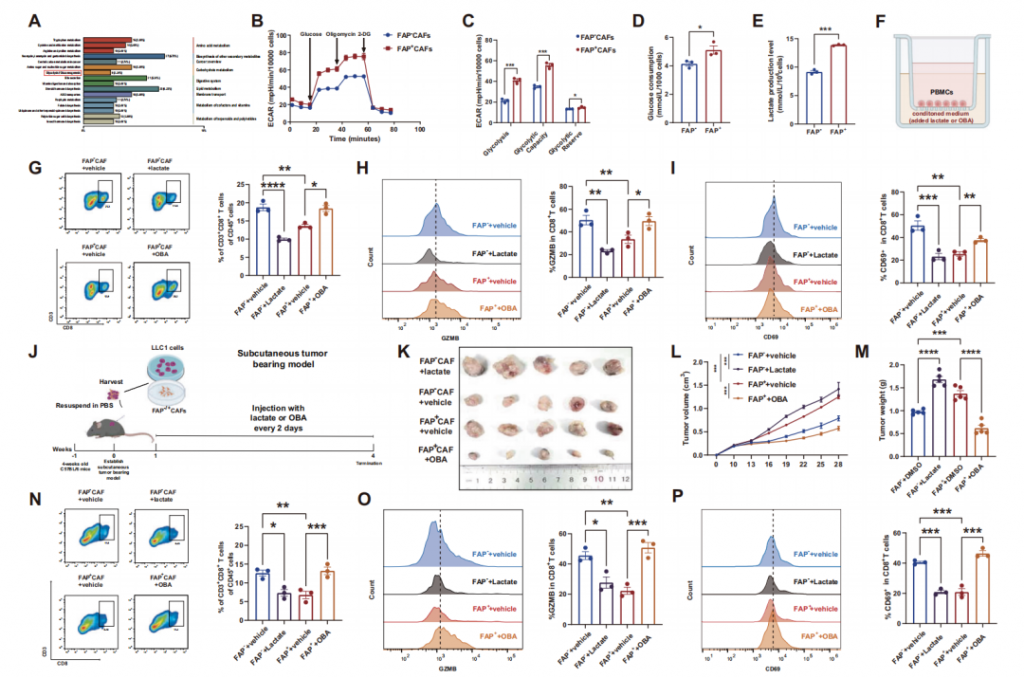
图2 FAP⁺ CAFs对CD8⁺T细胞的影响取决于其乳酸分泌失调
03 MCT4和LINC01711在FAP⁺CAFs的乳酸分泌异常中发挥关键作用
为探究成纤维细胞活化蛋白阳性癌症相关成纤维细胞乳酸异常的分子机制,实验发现MCT4(SLC16A3)在其体内显著上调,敲低该蛋白可减少细胞外乳酸分泌、增加细胞内蓄积,其抑制剂VB124可减慢肿瘤进展、降低乳酸水平并增加细胞毒性T淋巴细胞浸润,证实其通过该蛋白分泌乳酸。转录组测序显示,糖酵解关键酶基因无差异,而长链非编码RNA LINC01711上调最显著,仅敲低它可减少乳酸生成。组织芯片检测显示LINC01711与成纤维细胞活化蛋白共定位,且与细胞毒性T淋巴细胞呈负相关。进一步验证显示,LINC01711特异性高表达于该阳性亚型,其特征基因集与细胞毒性T淋巴细胞浸润正相关;LDHA高表达与肺腺癌不良预后相关,且筛选出MEIS3、TWIST1两个可能调控LINC01711的转录因子。
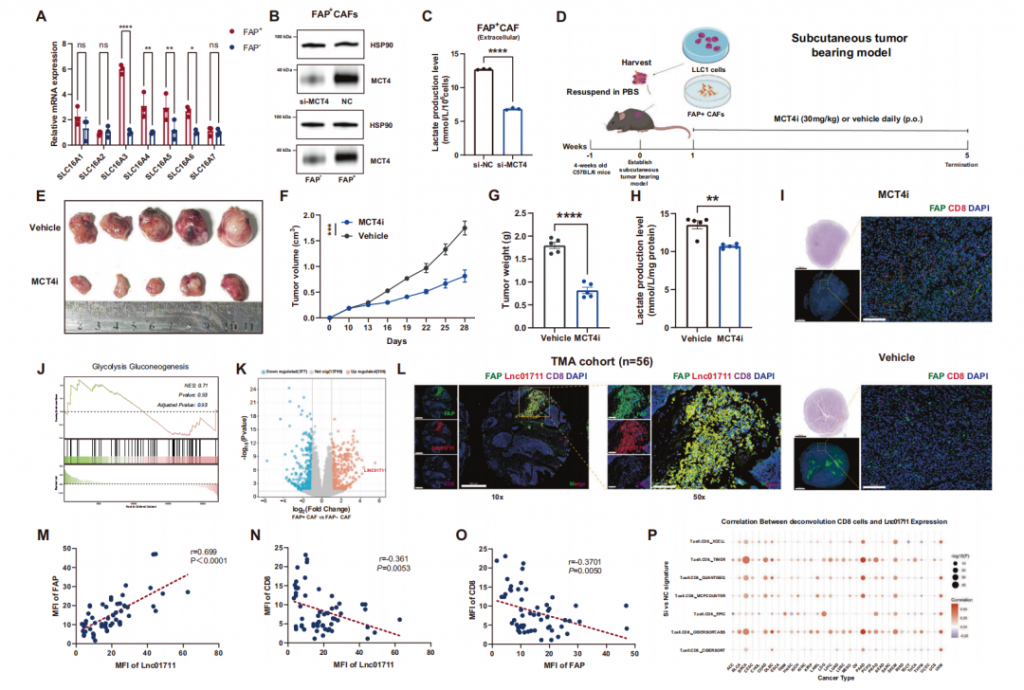
图3 MCT4和LINC01711在FAP⁺CAFs的乳酸分泌异常中发挥关键作用
04 LINC01711通过结合LDHA增强FAP⁺CAFs的有氧糖酵解
为验证LINC01711对 FAP⁺CAFs糖酵解的影响,敲低该RNA后,细胞外酸化率等实验证实其糖酵解能力及乳酸生成显著降低。因糖酵解关键酶编码基因无差异,排除其通过调控mRNA发挥作用,进一步实验证实LINC01711可特异性结合LDHA(不结合LDHB、 ALDOA),且二者在细胞质内存在空间相互作用。缺失突变体实验显示,LINC01711的1-348bp和820-967bp片段是结合关键区域;分子对接及突变体实验证实,LDHA的酪氨酸10位点是结合关键。综上,二者通过上述关键位点相互作用,增强该阳性亚型的有氧糖酵解。
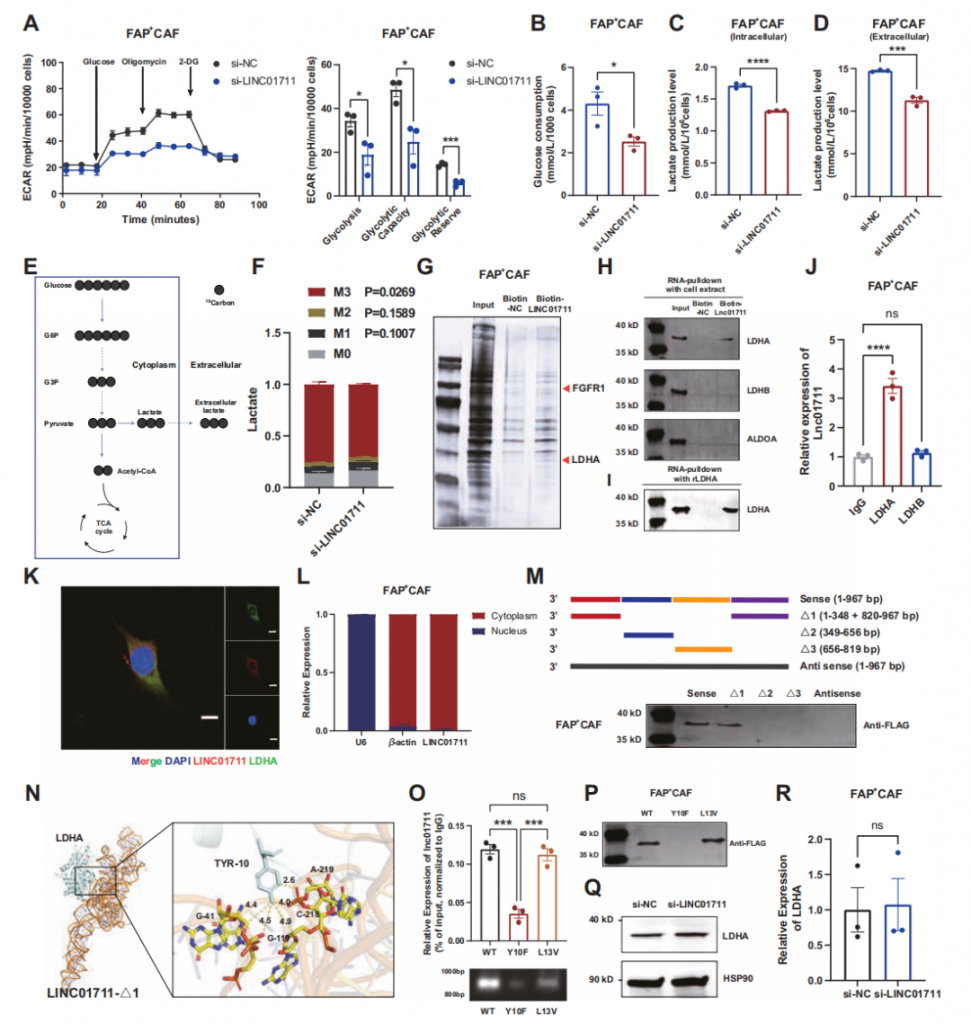
图4 LINC01711通过与LDHA结合增强有氧糖酵解
05 LINC01711通过FGFR1调控LDHA的磷酸化和四聚体形成
为探究LINC01711对LDHA生物学功能的调控机制,实验证实敲低LINC01711不影响LDHA的表达,但会显著降低其活性及酪氨酸10位点磷酸化水平(该位点调控其酶活性和四聚体形成)。进一步研究发现,敲低FGFR1或用其抑制剂PD166866处理,可显著降低LDHA酪氨酸10位点磷酸化,且LINC01711过表达会增强抑制剂作用。实验证实LINC01711可与FGFR1结合,且不影响其表达;敲低LINC01711会减弱FGFR1与LDHA的相互作用,体外激酶实验证实其能增强前者介导的后者磷酸化。此外,LINC01711过表达可依赖FGFR1,上调LDHA磷酸化水平并促进其活性四聚体形成,明确其调控LDHA功能的核心机制。
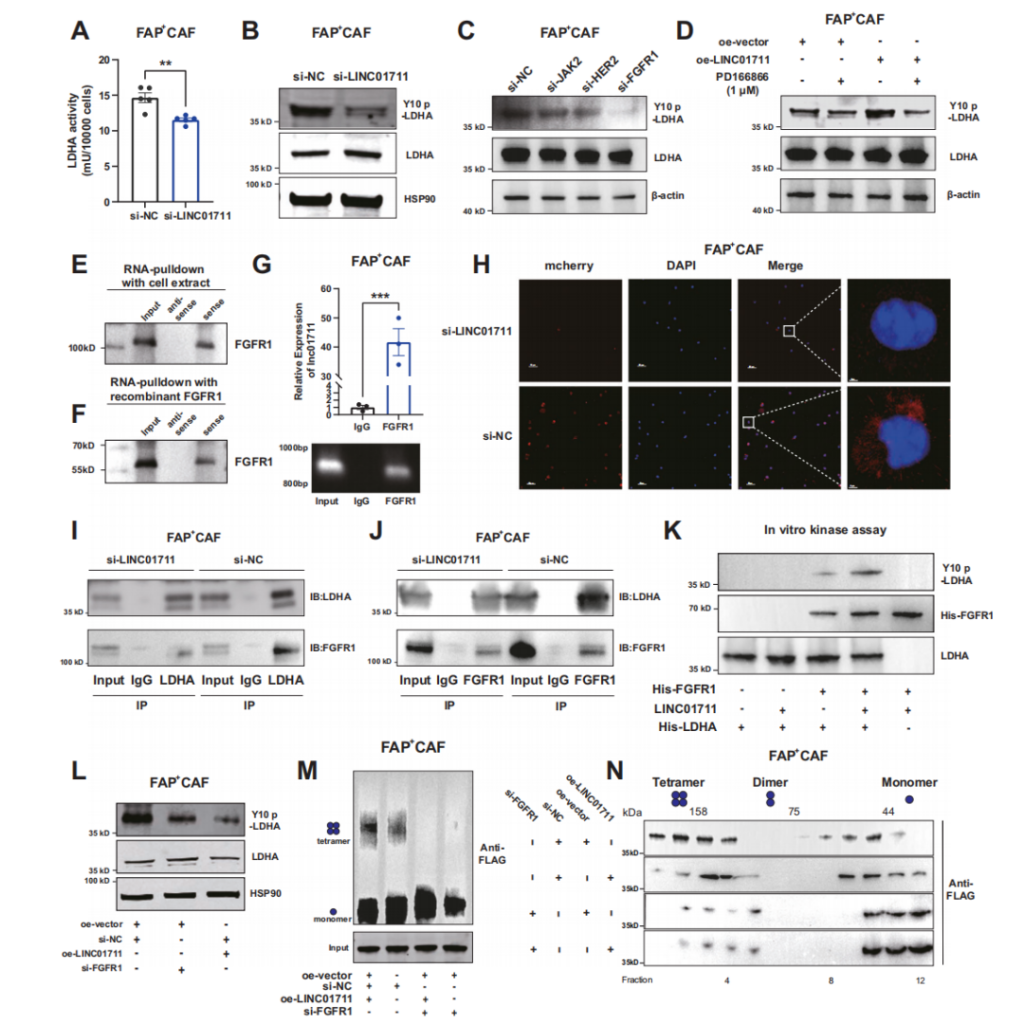
图5 LINC01711调节FGFR1对LDHA的磷酸化和四聚体形成
06 LINC01711通过FGFR1/LDHA复合物,增强FAP⁺CAFs的有氧糖酵解并保护其免受细胞毒性T淋巴细胞杀伤
实验首先证实,敲低FGFR1、抑制LDHA活性或转染其突变体,均不影响LINC01711表达。进一步验证显示,抑制LDHA活性后,LINC01711无法促进FAP+ CAFs有氧糖酵解;转染实验表明,敲低LINC01711仅影响野生型LDHA组糖酵解,对酪氨酸10苯丙氨酸突变体组无作用,且敲低FGFR1后,其调控作用消失。共培养及体内实验证实,敲低LINC01711可逆转该阳性亚型对细胞毒性T淋巴细胞杀伤的保护作用,而抑制LDHA活性后该作用消失,表明LINC01711通过调控LDHA活性,保护其免受细胞毒性T淋巴细胞杀伤。
07 基于LINC01711-siRNA系统,逆转FAP⁺CAFs介导的免疫逃逸并增强肺腺癌免疫治疗效果
实为探究敲低LINC01711能否逆转FAP⁺CAFs介导的免疫逃逸,实验发现其与LDHA抑制剂均能降低该阳性亚型糖酵解水平,且对於外周血单个核细胞糖酵解无显著影响,具潜在临床价值。本研究采用既往构建的小干扰RNA递送系统,将靶向LINC01711-siRNA(SC01711)通过尾静脉注射递送,证实其可有效敲低LINC01711并富集于肺组织,且无明显肝毒性和脱靶效应。肺腺癌原位移植模型显示,SC01711处理组肿瘤进展减慢、乳酸水平降低,细胞毒性T淋巴细胞浸润及毒性增加,小鼠生存期延长。进一步联合SC01711与抗PD-1抗体治疗,其抑瘤效果显著优于单药组,能进一步降低肿瘤乳酸水平、增强免疫浸润,证实该联合治疗在肺腺癌免疫治疗中具有潜在应用价值。
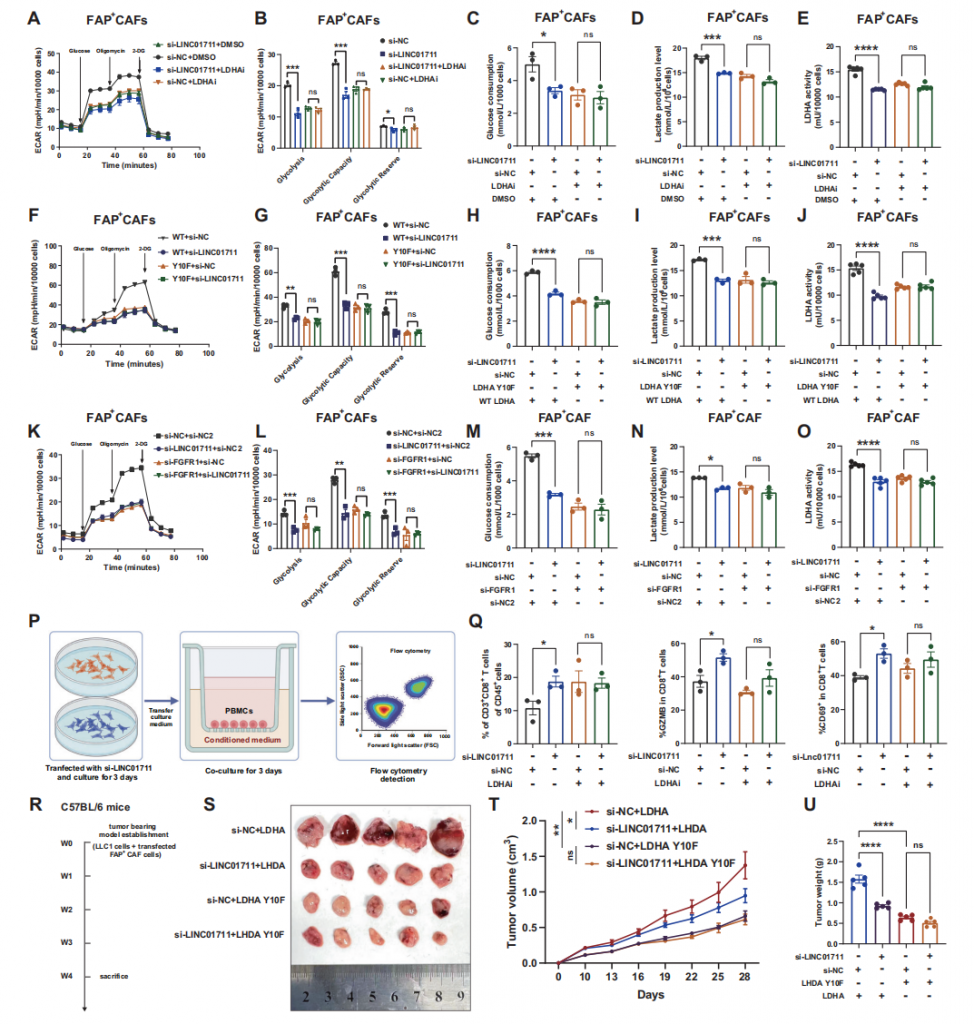
图6 LINC01711促进FAP⁺CAFs的需氧糖酵解,并通过FGFR1/LDHA复合物屏蔽CD8⁺T细胞攻击
研究总结
本研究发现,肺腺癌肿瘤微环境中,FAP⁺CAFs周围存在以乳酸为核心的化学屏障,该屏障会阻碍细胞毒性T淋巴细胞的浸润与功能发挥。进一步研究证实,FAP⁺CAFs特异性高表达长链非编码RNA LINC01711,该RNA通过促进FGFR1介导的LDHA在酪氨酸10位点的磷酸化,并推动其活性四聚体的形成,进而促进乳酸生成。随后FAP⁺CAFs通过MCT4将乳酸释放至肿瘤微环境,形成化学屏障并塑造免疫抑制性的肿瘤微环境。值得注意的是,本研究构建了基于小细胞外囊泡的体内自组装小干扰RNA递送系统,实现了对LINC01711的体内敲低,并证实该系统能显著提高肺腺癌对免疫检查点抑制剂的应答率。研究结果揭示了成纤维细胞活化蛋白阳性癌症相关成纤维细胞在介导肺腺癌对免疫检查点抑制剂耐药中的关键作用,并为克服该耐药问题提出了新型治疗策略。
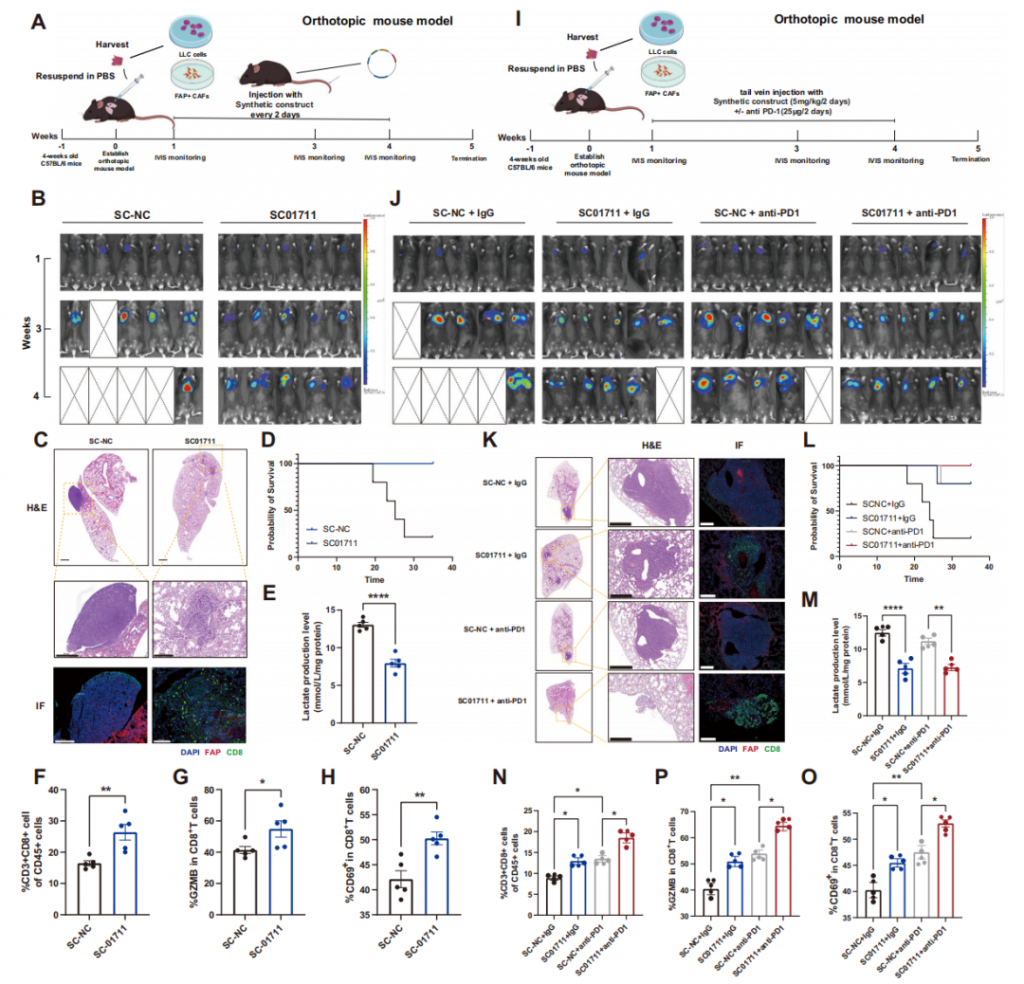
图7 利用sEVs在体内靶向LINC01711可逆转FAP⁺CAFs介导的免疫逃避,从而增强肺腺癌的免疫治疗效果



