科研前沿 | 多组学整合新突破!外周血代谢组+蛋白组联检,构建肿瘤免疫治疗无创预测模型

双buff加持,审稿人“暗戳戳”加分的小心机!
2026 年 1 月 12 日
IF:18.7 | 澳大利亚著名研究所联合南京农大在cell子刊发表小麦重要成果:4-氧代脯氨酸招募链霉菌,共筑抗旱防线
2026 年 1 月 15 日
肿瘤免疫治疗疗效的个体差异是当前科研与临床转化的核心瓶颈——如何早期、精准筛选优势获益人群,阐明疗效相关分子机制,是科研工作者亟待攻克的关键问题。
结合团队在多组学研究与肿瘤免疫领域的实践经验,整理分享一套「肿瘤免疫治疗疗效预测研究方法」,供各位老师参考借鉴。该方法以外周血为无创研究载体,整合代谢组、免疫因子蛋白组及生理指标多维度数据,通过ELISA等精准检测技术构建预测模型,可为肿瘤免疫治疗相关科研提供从样本设计到模型构建的完整思路框架。
疗效预测的“卡脖子”问题,多组学给出破局思路
尽管PD-1/PD-L1抑制剂等免疫治疗已成为恶性肿瘤治疗的重要方向,但临床转化中仍面临两大核心难题:
疗效评估滞后
一
传统RECIST标准依赖影像学观察肿瘤大小变化,无法早期预判疗效,难以满足机制研究与个体化治疗研究的需求;
分子机制不明
二
肿瘤-免疫互作的分子网络尚未完全解析,缺乏能精准关联疗效的核心生物标志物。
外周血作为无创、易获取的生物样本,其代谢组与蛋白组特征可直接反映肿瘤微环境与免疫系统的动态互作:代谢组能捕捉肿瘤增殖、免疫激活引发的全局代谢重编程;免疫因子蛋白组可精准量化PD-1/PD-L1、IFN-γ等关键调控分子的表达水平。二者联合整合,为突破疗效预测瓶颈、挖掘核心机制提供了全新的科研视角。
多组学整合+无创模型,完整技术路线
01 核心检测体系:代谢组与蛋白组
1. 样本预处理规范
采集:EDTA抗凝管(血浆)、促凝管(血清)各5mL,2h内冰袋冷藏转运;
分离:EDTA管4℃、3000r/min离心10min分血浆,促凝管静置30min后同条件分血清;
保存预处理:-80℃保存,避免反复冻融,检测前4℃解冻,标准化去蛋白/富集预处理。
2. 代谢组核心检测
非靶代谢组:全谱无偏探索,适配前期差异筛选,优势是发现未知差异,配套质控保障数据可靠;
靶向代谢组:已知差异物精准验证,高灵敏度/特异性,适配中期验证,可定制检测panel;
广靶代谢组:全谱覆盖+精准定量兼顾,适配筛选与验证衔接阶段,一次性完成“差异筛选-初步定量”,缩短研究周期。
3. 免疫因子蛋白组核心检测
靶向蛋白组:聚焦已知目标蛋白精准定量验证,适配核心免疫因子定量及标志物验证场景。
Olink蛋白组:高通量多因子筛查,适配大样本队列标志物初筛及多组学联合初筛场景。
空间蛋白组:解析蛋白空间分布,适配肿瘤微环境代谢-免疫空间关联及异质性研究场景。
全谱蛋白组:无偏性全蛋白发现,适配未知差异蛋白筛选及代谢-免疫通路全谱解析场景。
修饰蛋白组:聚焦蛋白翻译后修饰机制,适配免疫信号通路激活及代谢调控免疫功能研究场景。
4. ELISA辅助验证
目的:验证质谱差异免疫因子;
核心:筛选Fold Change>1.5、P<0.01的因子,标准化操作,结果与质谱相关性R²≥0.8。
5. 生理指标辅助检测
目的:排除急性炎症、肝肾功能异常等干扰;
检测指标:血常规、炎症指标(CRP等)、肝肾功能核心指标。
02研究设计与分析流程
核心逻辑:“差异筛选-机制挖掘-模型构建-验证转化”
1. 分组设计
纳入肿瘤免疫治疗患者(根据RECIST 1.1标准分为有效组和无效组)及年龄性别匹配健康对照组;每组≥30例,保障基线均衡,减少混杂因素。
2. 核心数据预处理
用Progenesis QI(代谢组)、MaxQuant(蛋白组)处理原始数据;进行缺失值填充(代谢组KNN/蛋白组最小值)、Z-score标准化;剔除RSD>15%的不合格数据。
3. 差异分子筛选
通过t检验/ANOVA(P<0.05、Fold Change>1.2或<0.83)+LASSO回归筛选;获得20-30种差异代谢物、10-15种差异免疫因子核心集。
4. 核心机制挖掘
联合功能富集分析:代谢组KEGG(糖酵解等通路),蛋白组GO+KEGG(免疫调节相关通路);明确“代谢重编程-免疫调控”协同机制。
5. 多维度预测模型构建与优化
以核心差异分子+少量临床指标为变量,用RF、SVM、LR、NN算法构建模型;五折交叉验证优化,通过ROC、AUC等评估,筛选最优模型(预期AUC≥0.85,准确率≥80%)。
6. 模型验证与可靠性评估
采用内部验证(30%验证集)+外部验证(独立队列);评估模型稳定性、泛化能力及临床应用价值。
案例分享(一)

肝癌联合免疫治疗疗效预测
该研究针对不可切除肝癌患者的伦伐替尼+抗 PD1 联合治疗,整合血浆非靶代谢组、Label-free蛋白组及全外显子测序数据,发现治疗应答者具有高肿瘤突变负荷(TMB)、补体通路激活及溶血磷脂酰胆碱(LysoPCs)升高的特征,而非应答者则富集免疫球蛋白相关蛋白。基于代谢组特征构建的逻辑回归和随机森林模型,在训练集、验证集中均展现优异预测性能(AUC最高达1.0),且能跨癌种(肾癌)验证,为肝癌联合免疫治疗提供了无创、精准的疗效预测标志物及 “代谢-免疫” 协同调控机制,为个体化治疗策略制定提供关键支撑。
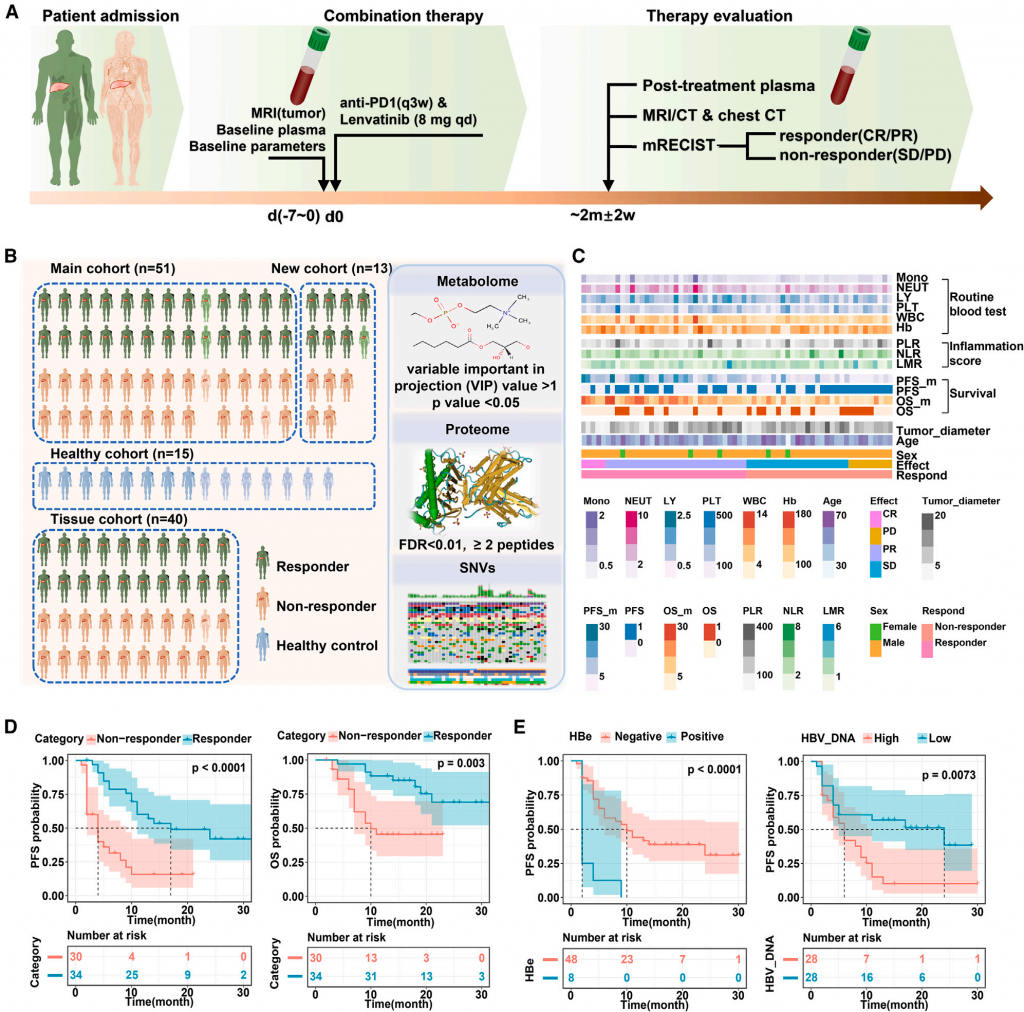
图1 接受抗PD1联合仑伐替尼治疗的HCC患者血浆蛋白质组与代谢组的分子特征分析
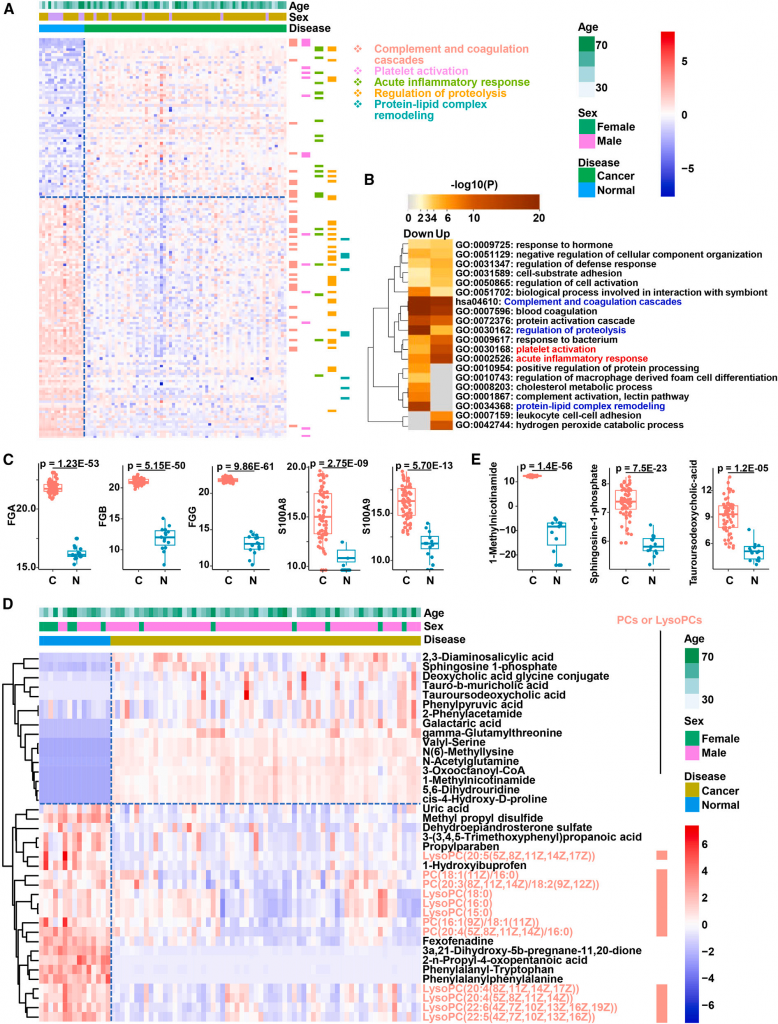
图7 肝细胞癌与正常对照组间的差异性血浆蛋白及代谢物
案例分享(二)

非小细胞肺癌 PD-(L) 1 抑制剂疗效与安全性预测
该研究采用Olink免疫肿瘤学panel(92种蛋白)对非小细胞肺癌患者血浆进行蛋白组学分析,发现PD-(L)1抑制剂治疗后42种蛋白显著上调(富集于细胞因子-受体相互作用、趋化因子信号通路),并筛选出应答相关(如TNF、CXCL10)及免疫相关不良反应(irAE)相关(如IL-4、IL-13)核心蛋白。通过LASSO-Cox回归构建的I-SCORE风险模型,基于8种关键蛋白实现对患者总生存期、无进展生存期及治疗应答的精准预测,且高评分与患者炎症及免疫抑制表型密切相关,证实了血浆蛋白组学作为液体活检工具在免疫治疗疗效与安全性预判中的可靠性,为临床筛选优势获益人群提供了实用工具。
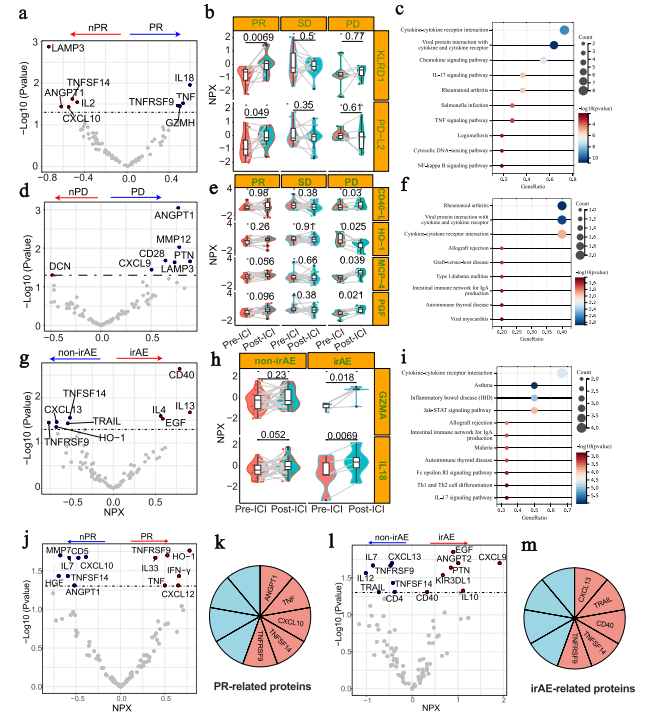
图3 根据ICI治疗反应和毒性的血浆蛋白质组学分析



