项目文章 | 太空也会“伤脑”?顶刊研究破解微重力致认知下降元凶,亚油酸成航天脑保护新密钥!

J Hazard Mater(IF:11.3) | 山东省农业科学院为有机硒提升玫瑰抗病性提供新的科学依据
2026 年 3 月 17 日
救命!葡萄香气淡到没味道?Horticulture Research揭秘:是这些分子标记在“拖后腿”
2026 年 3 月 23 日
长期太空飞行中,微重力会导致宇航员返回后认知下降、焦虑难消,且短时间难以恢复,成为航天医学重大难题。传统研究多聚焦神经、骨骼、肌肉损伤,却忽略肠-脑轴这一核心通路。
近日,空军军医大学团队在Gut Microbes(IF=11)发表重磅研究,首次完整阐明模拟微重力通过干扰“保护性菌群代谢物–小胶质细胞”信号诱发脑功能障碍的机制,并证实亚油酸(LA)可同步修复肠道与大脑,为航天健康防护提供全新策略。
百谱生物为该研究提供了代谢组检测服务!

文章题目:Simulated microgravity induces cerebral dysfunction by disturbing protective microbiota-metabolite-microglia signaling across the gut-brain axis
期刊名称:Gut Microbes
影响因子:11
发表时间:2026年2月
研究方法:16S rRNA测序、非靶代谢组、靶向代谢组等
发表单位:空军军医大学航空航天医学系等
研究思路:
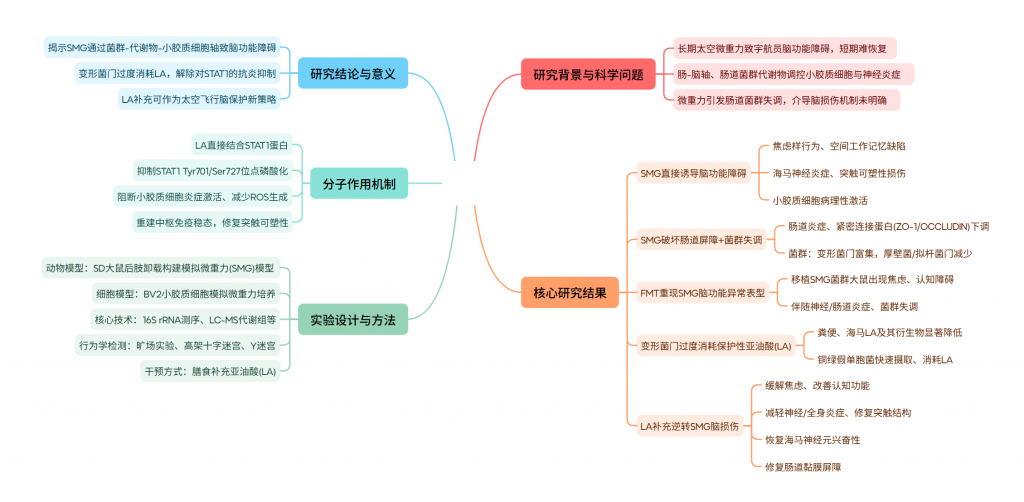

本研究选用SPF级雄性SD大鼠构建动物模型,采用后肢悬吊法建立28天模拟微重力(SMG)模型,以水平尾悬吊大鼠作为正常重力(NG)对照;体外细胞实验采用小鼠小胶质细胞系BV2,通过双轴旋转生物反应器模拟10⁻³G太空微重力环境。研究中通过抗生素鸡尾酒耗竭肠道菌群,结合粪菌移植(FMT)验证菌群的核心介导作用;利用16S rRNA测序分析肠道菌群结构,非靶向与靶向LC-MS代谢组筛选关键差异代谢物;同时采用qRT-PCR、免疫印迹、免疫荧光、透射电镜、高尔基染色检测组织病理、蛋白表达与突触超微结构,全细胞膜片钳记录海马CA1锥体神经元电生理活性,分子对接与表面等离子共振(SPR)验证分子互作;通过旷场实验、高架十字迷宫、Y迷宫完成大鼠行为学评估,所有实验均设置独立生物学重复并进行严格统计学分析。

01 表型验证:微重力诱导脑功能障碍并伴随突触损伤
采用大鼠后肢悬吊28天构建模拟微重力模型,通过行为学、分子病理及电镜检测,从“行为异常-神经炎症-突触结构”多维度验证微重力对脑功能的损伤作用。
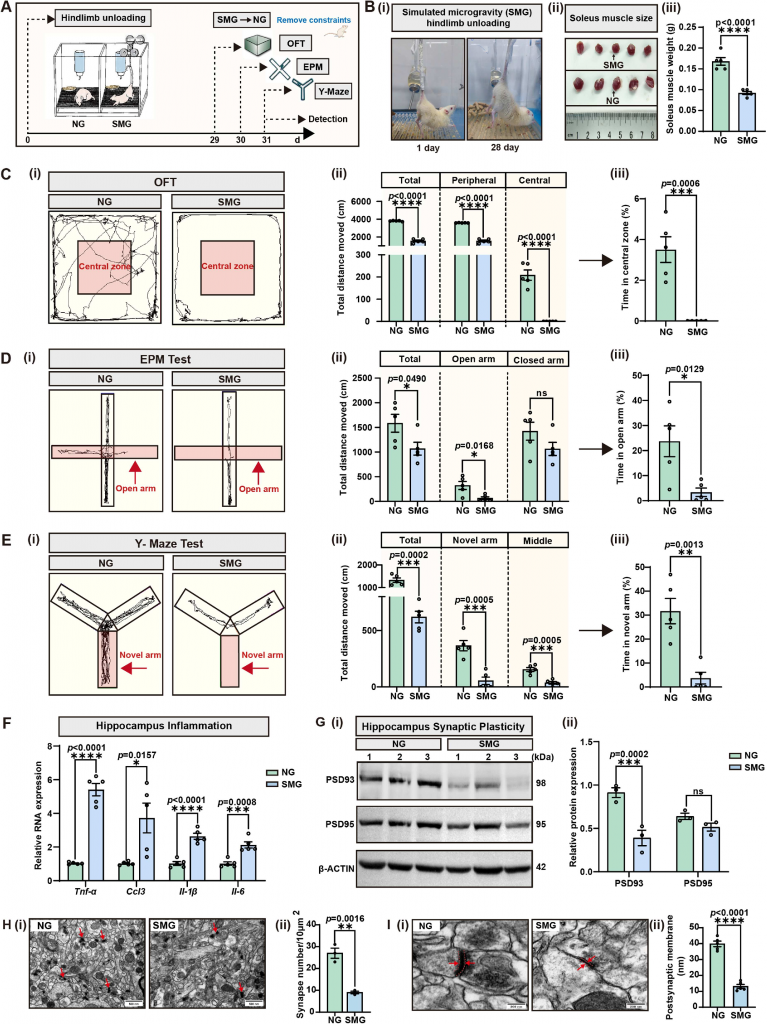
图1 SMG通过损害突触可塑性诱导认知功能障碍
长期模拟微重力可诱发大鼠出现显著的焦虑样行为与空间工作记忆障碍,同时海马区促炎因子TNF-α、IL-1β、IL-6等表达显著上调,神经炎症反应剧烈,透射电镜观察到突触密度降低、突触后膜厚度变薄,突触超微结构严重受损;而清除小胶质细胞后,微重力诱导的神经炎症与行为异常可得到明显缓解,证实小胶质细胞的病理性激活是微重力引发脑功能障碍的核心环节。
02 肠道损伤:微重力破坏肠屏障并诱导促炎型菌群失调
对模拟微重力处理后的大鼠进行结肠组织病理、肠道屏障蛋白及16S rRNA测序分析,探究微重力对肠道结构与菌群的影响。
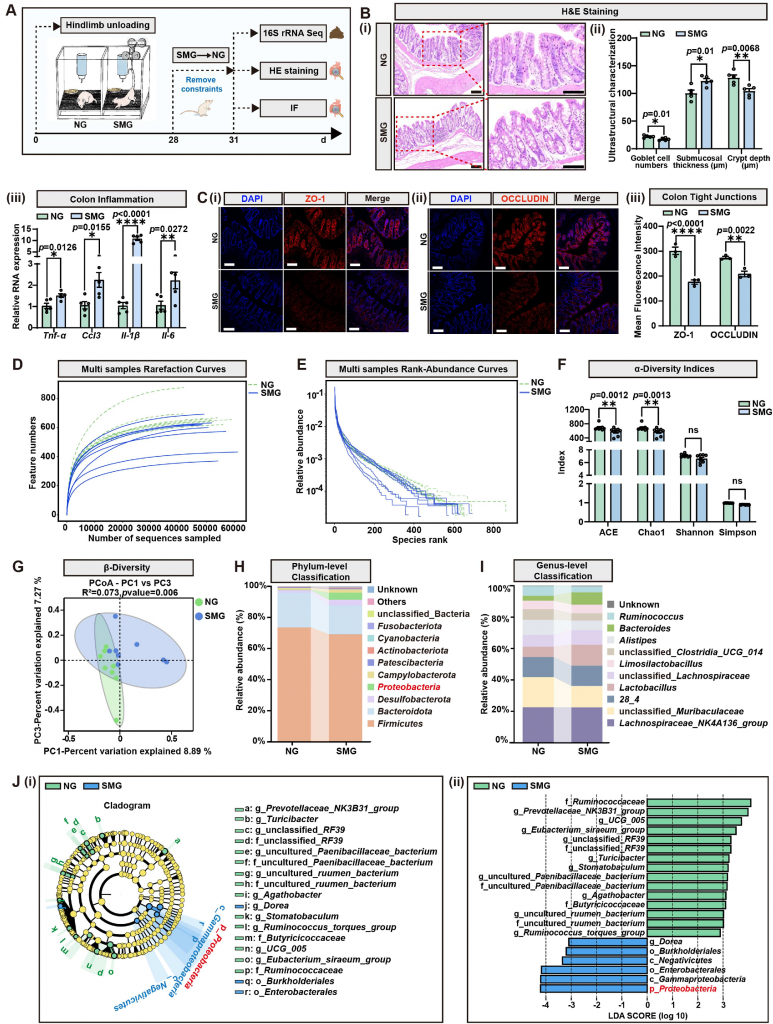
图2 SMG触发变形菌门扩张、肠道屏障功能障碍及微生物群失调
模拟微重力会严重破坏肠道屏障完整性并引发肠道菌群失调,结肠组织出现明显炎症损伤,紧密连接蛋白ZO-1与Occludin表达显著降低,肠道通透性升高;16S rRNA测序表明菌群α多样性下降,有益的厚壁菌门、拟杆菌门丰度减少,促炎的变形菌门显著富集,成为微重力干预后最具标志性的差异菌群,且这种异常菌群状态在恢复正常重力后无法快速逆转。
03 粪菌移植:微重力紊乱菌群可直接传递脑损伤表型
将模拟微重力处理大鼠的粪便移植给正常重力大鼠,通过行为学、病理及菌群检测,验证肠道菌群对脑功能的介导作用。
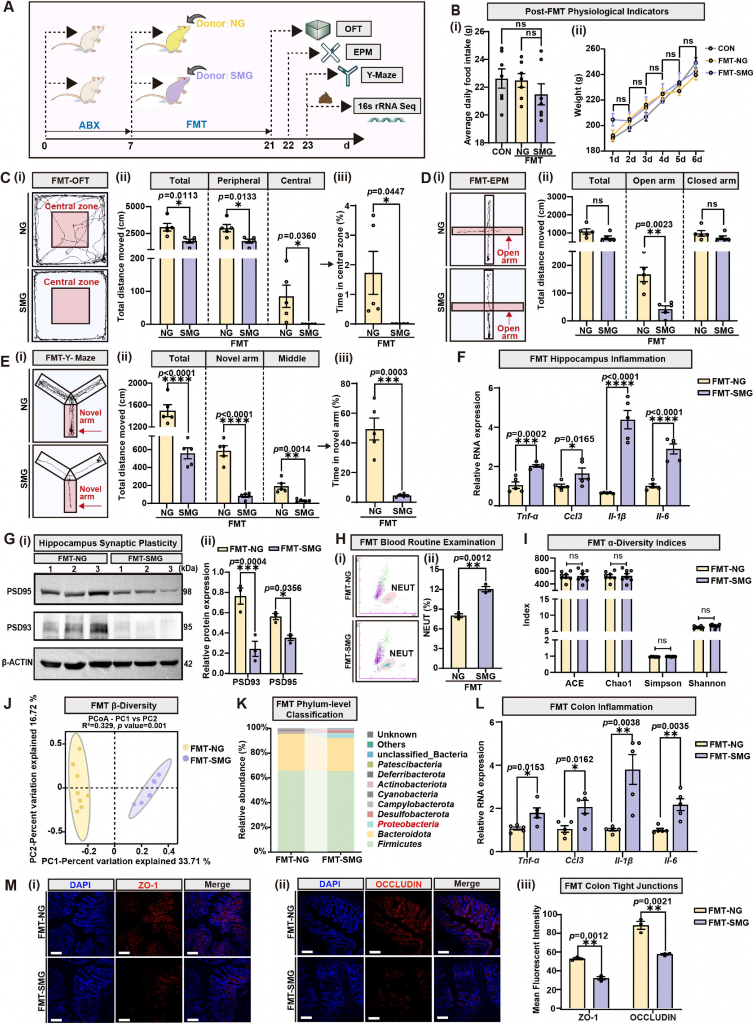
图3 FMT-SMG可诱导与SMG相似的脑功能障碍
粪菌移植后的受体大鼠可完全重现供体鼠的焦虑样行为、认知缺陷、肠道炎症、菌群紊乱等表型,同时海马区出现与供体一致的神经炎症与突触损伤,充分说明肠道菌群是介导微重力诱导脑功能障碍的核心媒介,紊乱的菌群可独立触发肠-脑轴损伤。
04 代谢筛选:微重力促使变形菌门过度消耗保护性亚油酸
采用非靶向与靶向代谢组学结合微生物组关联分析,筛选微重力干预下肠-脑轴关键差异代谢物。
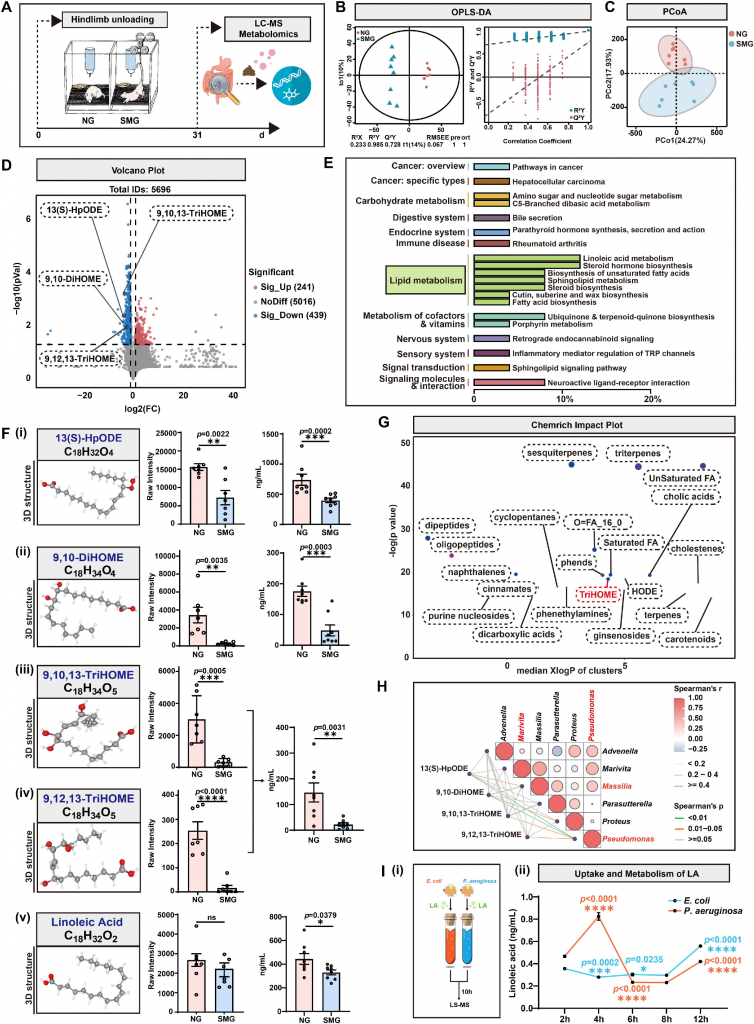
图4 proinflammatoryProteobacteriaunder SMG条件下,保护性LA的消耗速率加快
模拟微重力会显著改变肠道代谢谱,其中脂质代谢通路出现剧烈紊乱,保护性代谢物亚油酸(LA)及其衍生物水平大幅下降;菌群与代谢组关联分析及体外细菌实验进一步证实,微重力富集的变形菌门尤其是铜绿假单胞菌,可快速摄取并大量消耗LA,直接导致机体保护性代谢物匮乏,中断肠-脑轴保护性信号。
05 干预验证:补充亚油酸同步逆转肠道损伤与脑功能障碍
通过饲料添加10%亚油酸对模拟微重力大鼠进行干预,检测肠道、行为及脑内病理与功能变化。
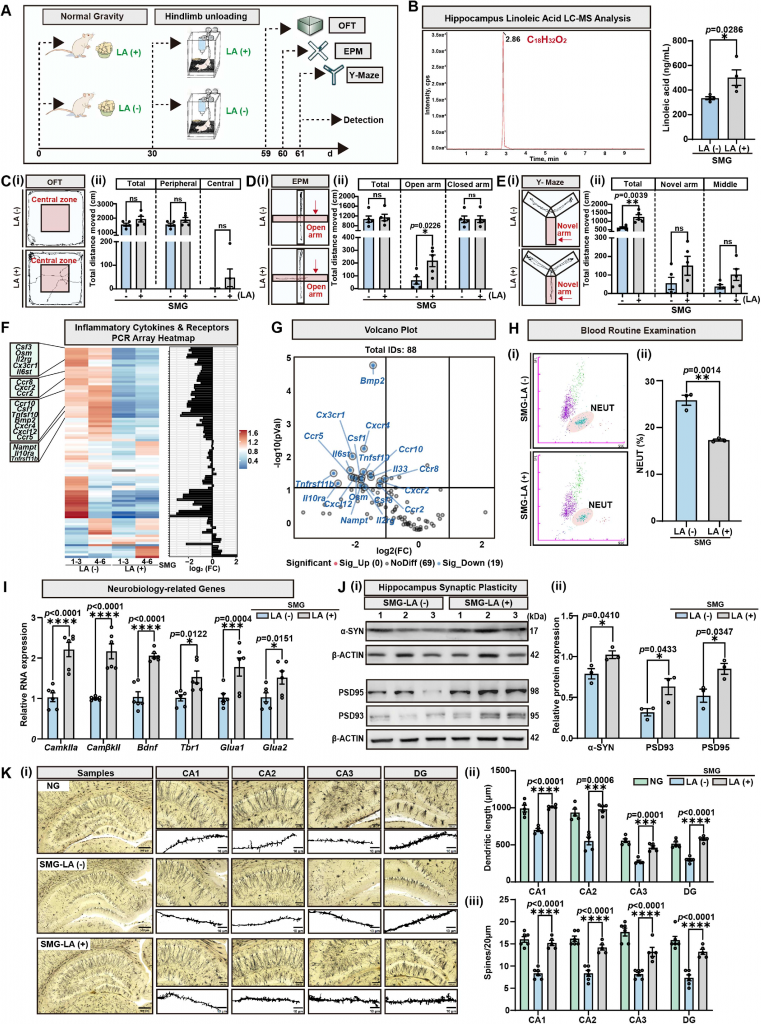
图5 LA补充剂通过增强海马突触可塑性缓解SMG诱导的脑功能障碍
膳食补充亚油酸能够有效修复肠道屏障、减轻结肠炎症,同时显著改善大鼠的焦虑样行为与空间认知障碍,恢复海马区突触结构与神经可塑性相关蛋白表达,降低全身及中枢神经炎症水平,实现肠道与大脑的同步保护。
06 电生理证实:亚油酸恢复微重力受损的海马神经元兴奋性
采用全细胞膜片钳技术,检测模拟微重力及亚油酸干预后海马CA1区锥体神经元的电生理活性。
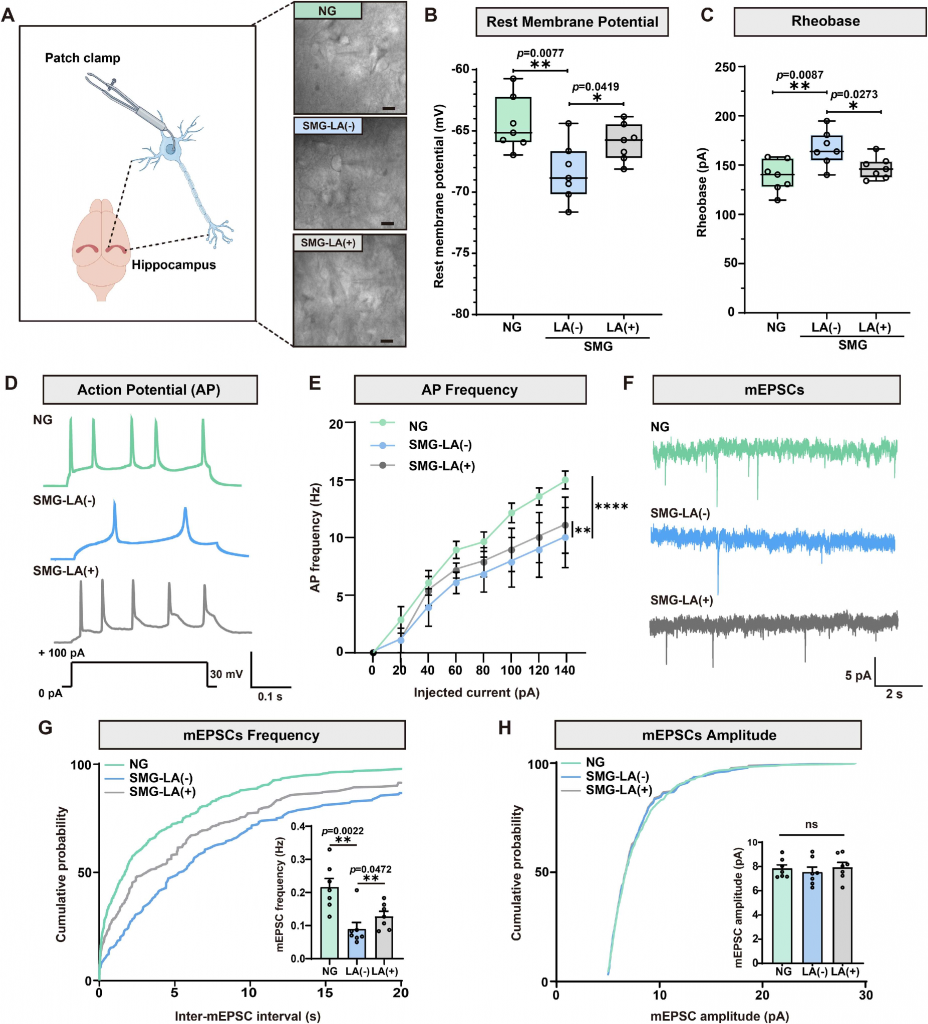
图6 SMG大鼠给予LA后海马CA1区锥体神经元电生理学改变
模拟微重力会显著降低海马CA1区锥体神经元的兴奋性,导致神经元静息电位异常、动作电位发放减少、微小兴奋性突触后电流频率降低;而亚油酸补充可有效逆转上述电生理异常,从神经功能层面验证其对微重力损伤大脑的修复作用。
07 机制阐明:亚油酸靶向STAT1通路抑制小胶质细胞炎性激活
通过分子对接、SPR及分子生物学实验,探究亚油酸保护神经的核心分子机制。
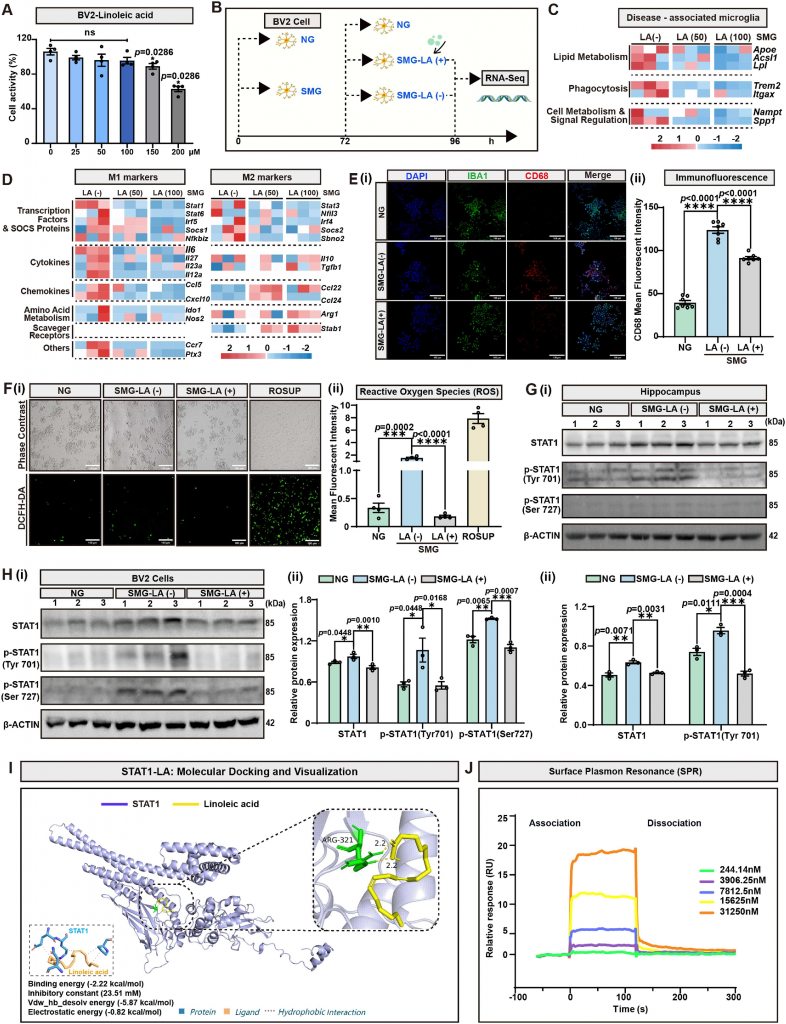
图7 LA抑制炎症小胶质细胞的活化
亚油酸可直接结合STAT1蛋白,并特异性抑制其在Tyr701与Ser727位点的磷酸化激活,进而阻断小胶质细胞的促炎性极化,减少活性氧生成与神经炎症因子释放,从分子层面明确了亚油酸调控肠-脑轴、发挥神经保护作用的关键通路。

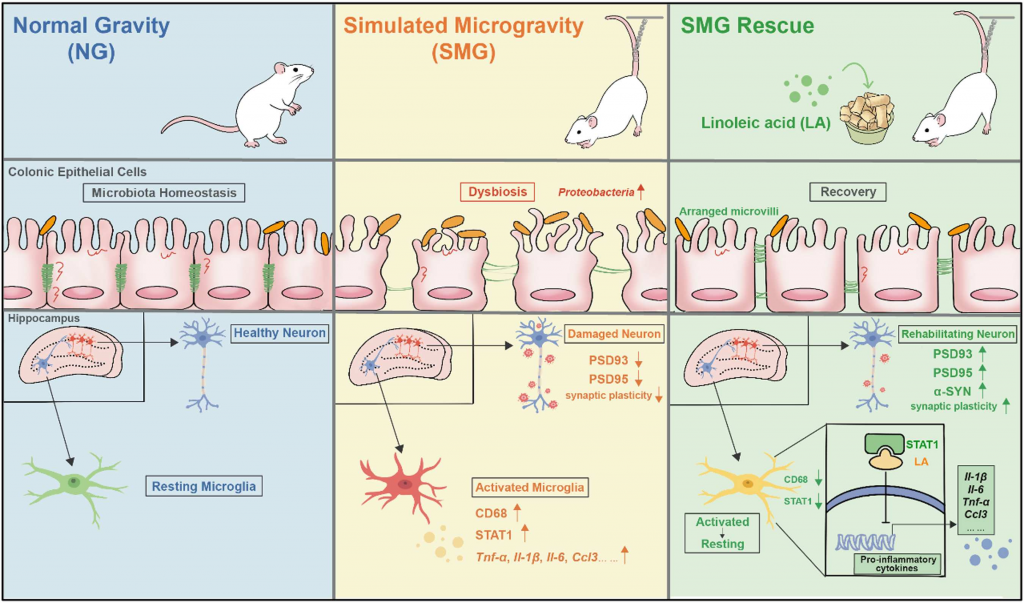
模拟微重力→肠屏障损伤+肠道菌群失调→促炎变形菌门富集→过度消耗保护性亚油酸(LA)→循环中LA 不足、海马LA缺乏→STAT1过度磷酸化激活→小胶质细胞病理性促炎活化→海马神经炎症+突触结构/功能损伤→焦虑样行为+认知功能障碍。
补充LA→恢复肠–脑轴LA水平→直接结合并抑制STAT1→平息小胶质细胞炎症→修复突触与神经元功能→同步改善肠道损伤与脑功能障碍。




