顶刊方案|多组学锁定畜禽肠道健康标志物,肠源性疾病早预警

破解食管癌地域性高发之谜!中国科学家绘制化学暴露组全景图,为早期筛查开辟新路径
2026 年 1 月 21 日
3分钟吃透转录组+蛋白质组+代谢组学高分期刊核心机制
2026 年 1 月 27 日
📌肠道健康是畜禽养殖的“隐形基石”,肠源性疾病频发常导致畜禽死亡率升高、饲料转化率下降,造成巨大经济损失,同时抗生素滥用引发的耐药性问题也加剧行业困境。本次分享的全景评估方案,以中科院1区《Microbiome》(IF=12.7)高分文献为核心支撑,融合代谢组、微生物组、宏基因组多组学技术,实现肠源性疾病标志物精准筛选与健康状态全景评估,覆盖多畜禽物种、全流程检测,既适用于科研项目设计,也可落地于养殖行业实操应用。
研究背景
肠道作为畜禽最大的消化吸收器官和免疫屏障,其健康状态直接决定畜禽生产性能、抗病能力及产品安全性。单一组学技术难以揭示“菌群-代谢物-宿主健康”的复杂互作机制,而多组学联合分析可实现全景解析,为肠源性疾病早期预警提供新路径。
以顶刊为支撑,兼顾科研严谨性与产业实用性,突破单组学研究局限性
材料与方法:
1. 研究对象与实验设计:
以雏鸡、仔猪为核心研究对象,同步扩展至肉牛、肉羊等畜禽,覆盖禽类、哺乳类代表性物种。设置健康对照组与肠源性疾病试验组,每组生物学重复≥10个,配套平行组与验证组。统一标准化饲养环境与管理流程,消除混杂因素干扰,试验周期按物种调整为2-8周。
2. 样本采集与处理:
①样本类型:覆盖三大类核心样本——微生物分析(粪便、各肠段内容物)、代谢组分析(血浆/血清、肠黏膜组织)、宿主验证(肠黏膜及外周组织);
②处理方法:样本采集后液氮速冻、-80℃保存,微生物样本提取总DNA/RNA,代谢组样本经萃取去蛋白处理,组织样本分样适配多维度检测需求。
3. 检测技术方法:
①微生物组:采用16S rRNA/ITS扩增子测序,覆盖细菌、真菌,解析物种组成与多样性;
②宏基因组:鸟枪法测序结合NGS+TGS混合组装,重构cMAGs,筛查功能基因与代谢通路;
③代谢组:“非靶向(LC-MS/MS/GC-MS)+靶向(MRM技术)” 联合检测,精准定性定量核心代谢物。
4. 数据分析方法:
单组学层面:筛选差异物种、代谢物及功能基因(P<0.05,FDR<0.1);
多组学层面:通过CCA、Spearman相关性分析构建互作网络,结合随机森林等算法筛选标志物;最后经“分子-细胞-动物”三级验证保障结果可靠。
技术体系全覆盖,适配不同样本、物种及检测需求,数据分析流程对标顶刊标准
文章案例及实验结果

文章题目:Gut microbiome-derived indole-3-carboxaldehyde promotes intestinal development via AHR-NRF2 signaling in the early-life of chicks
期刊名称:Microbiome
影响因子:12.7
发表时间:2025年12月
发表单位:华中农业大学等
研究方法:微生物学+宏基因组+代谢组学等
肠道菌群与宏基因组特征:乳杆菌是肠道健康 “核心卫士”
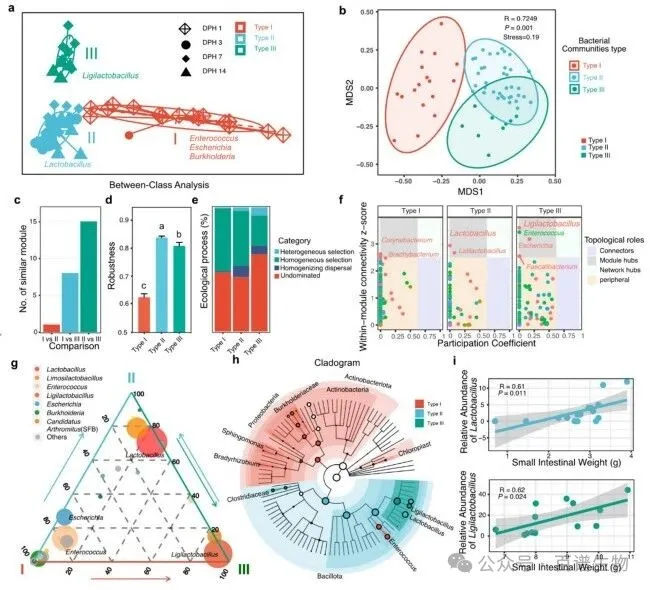
图2 乳杆菌属与双歧乳杆菌属是与肠道成熟相关的优势菌属
健康畜禽的肠道菌群从3日龄后就进入稳定期,厚壁菌门占绝对主导,其中乳杆菌属、连接乳杆菌属会持续富集。而疾病组的菌群多样性明显降低(P<0.05),这些有益菌的丰度大幅下降,致病菌却增多。
代谢组差异特征:IAld与ICA为肠道健康关联特征代谢物
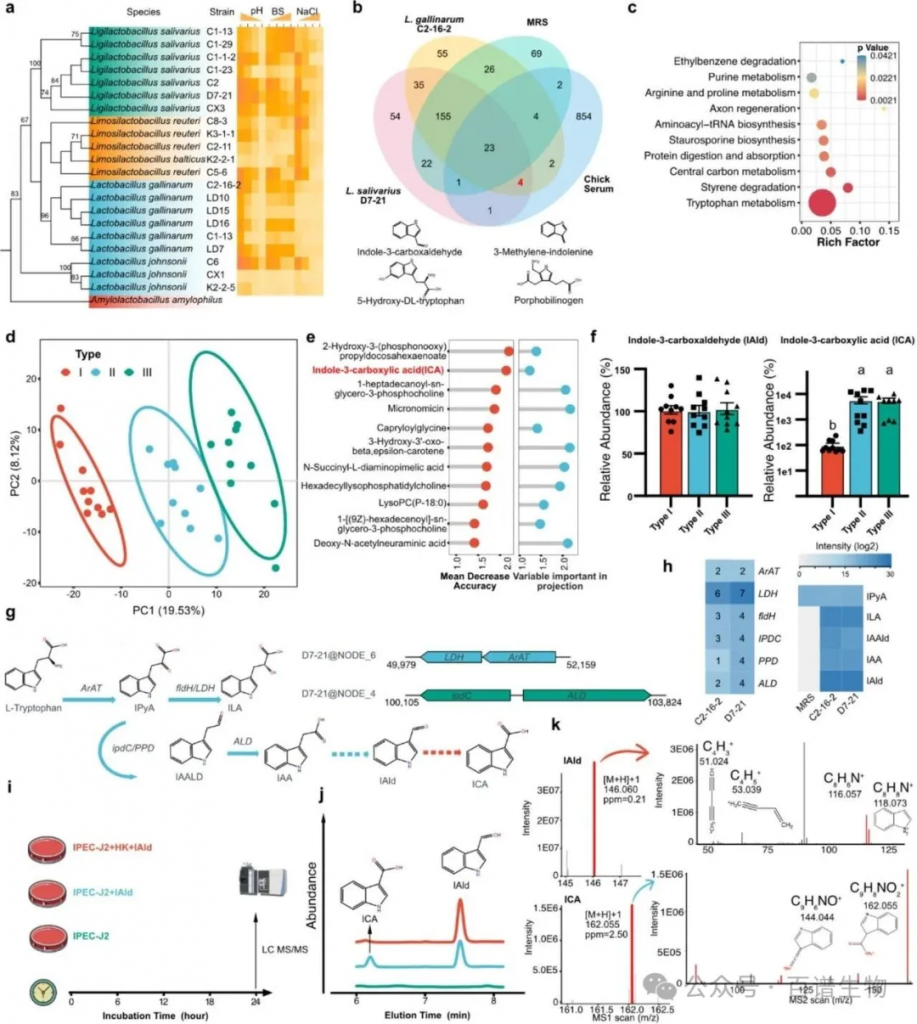
图3 不同类型细菌群落中特征菌株及代谢产物的鉴定
非靶向代谢组分析鉴定出菌株发酵液与鸡血清共有代谢物4种,其中3种参与色氨酸代谢,通路富集分析显示差异代谢物主要集中于色氨酸代谢通路。PLS-DA分析表明,3种菌群分型的血清代谢组存在显著分离,随机森林与OPLS-DA VIP评分联合筛选出吲哚-3-羧酸(ICA)为核心差异代谢物。定量分析显示,Type II/III血清中ICA丰度显著高于Type I,而吲哚-3-甲醛(IAld)丰度无显著组间差异。菌株基因组测序证实,L.gallinarum C2-16–2与L.salivarius D7-21携带完整的色氨酸代谢基因簇(ArAT、LDH、IPDC、ALD),可体外合成IAld;IPEC-J2细胞试验与酶学验证表明,IAld可通过黄嘌呤脱氢酶催化转化为ICA,且ICA体外生物活性高于IAld。
特征菌株与代谢物对雏鸡肠道健康的体内验证
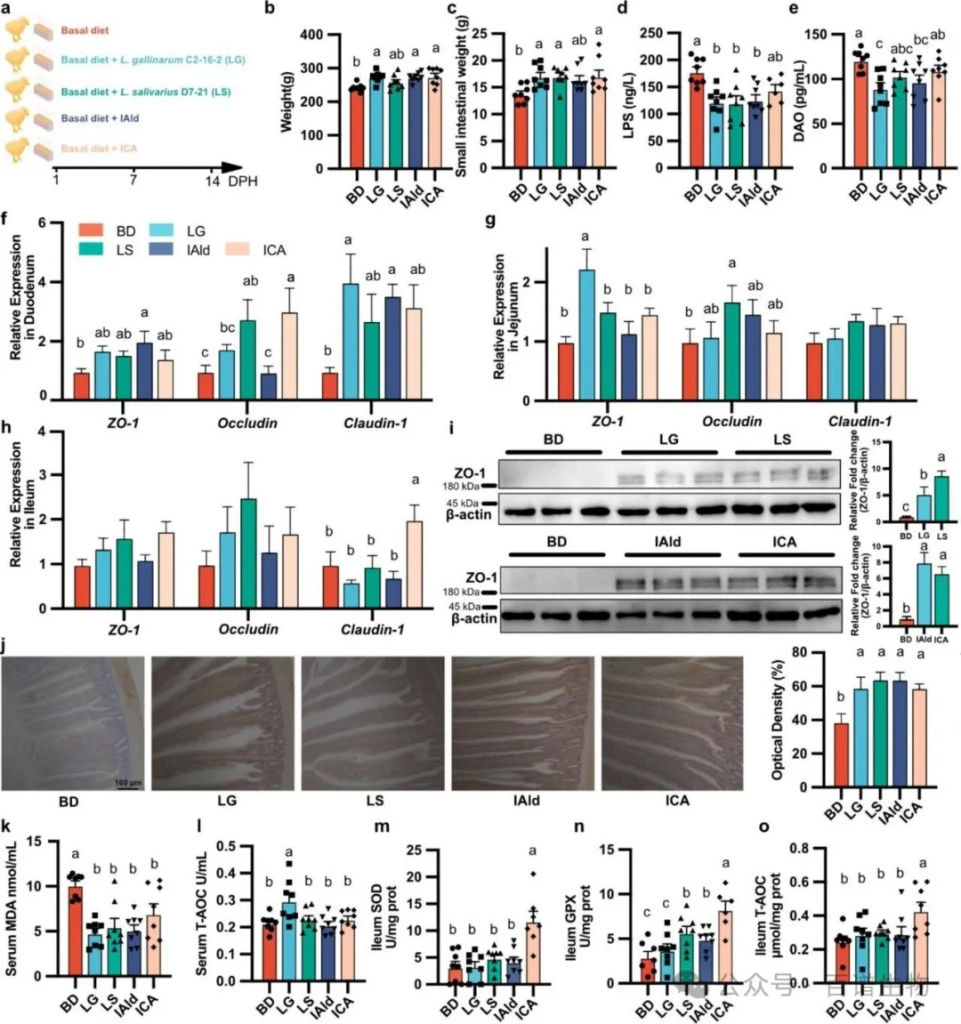
图4 L. gallinarum、L. salivarius及其衍生的IAld与ICA对雏鸡小肠发育影响的验证
动物饲喂试验显示,LG、LS、IAld、ICA处理组14日龄雏鸡体重及小肠重量显著高于基础日粮组,血清LPS、DAO水平显著降低。RT-qPCR结果显示,LS组显著上调十二指肠和空肠Occludin表达,LG组显著上调空肠ZO-1表达,ICA组显著上调十二指肠Occludin及回肠Claudin-1表达;WB及免疫组化证实,各处理组十二指肠、空肠ZO-1蛋白表达均显著升高。抗氧化指标检测显示,各处理组血清MDA浓度显著降低,LG组血清T-AOC显著升高,LS和ICA组回肠GPX活性显著提升。
IAld/ICA缓解LPS诱导的IPEC-J2细胞屏障损伤
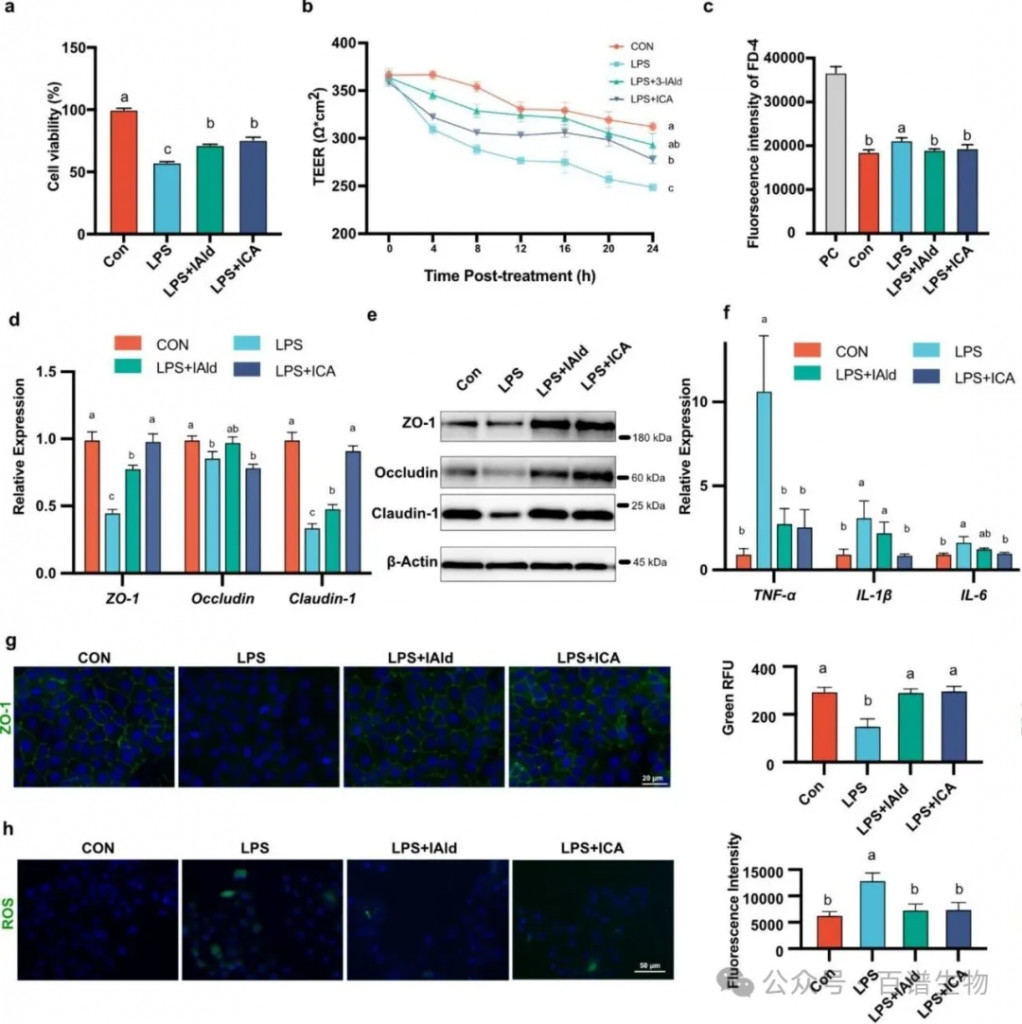
图5 L. gallinarum和L. salivarius来源的IAld/ICA可改善肠道上皮屏障功能,并在LPS诱导模型中减轻炎症和氧化反应
LPS诱导IPEC-J2细胞损伤后,50μM IAld和5μM ICA预处理可显著提升细胞活力、TEER值,降低FD-4通透性。分子水平上,IAld/ICA处理显著上调ZO-1、Claudin-1 mRNA及蛋白表达,并显著降低TNF-α、IL-1β、IL-6炎症因子mRNA水平。免疫荧光显示,IAld/ICA可改善LPS诱导的ZO-1蛋白分布紊乱,同时显著降低细胞内ROS水平,证实其对肠道上皮屏障的保护及抗炎抗氧化活性。
IAld/ICA通过激活AHR-NRF2通路调控肠道健康的机制
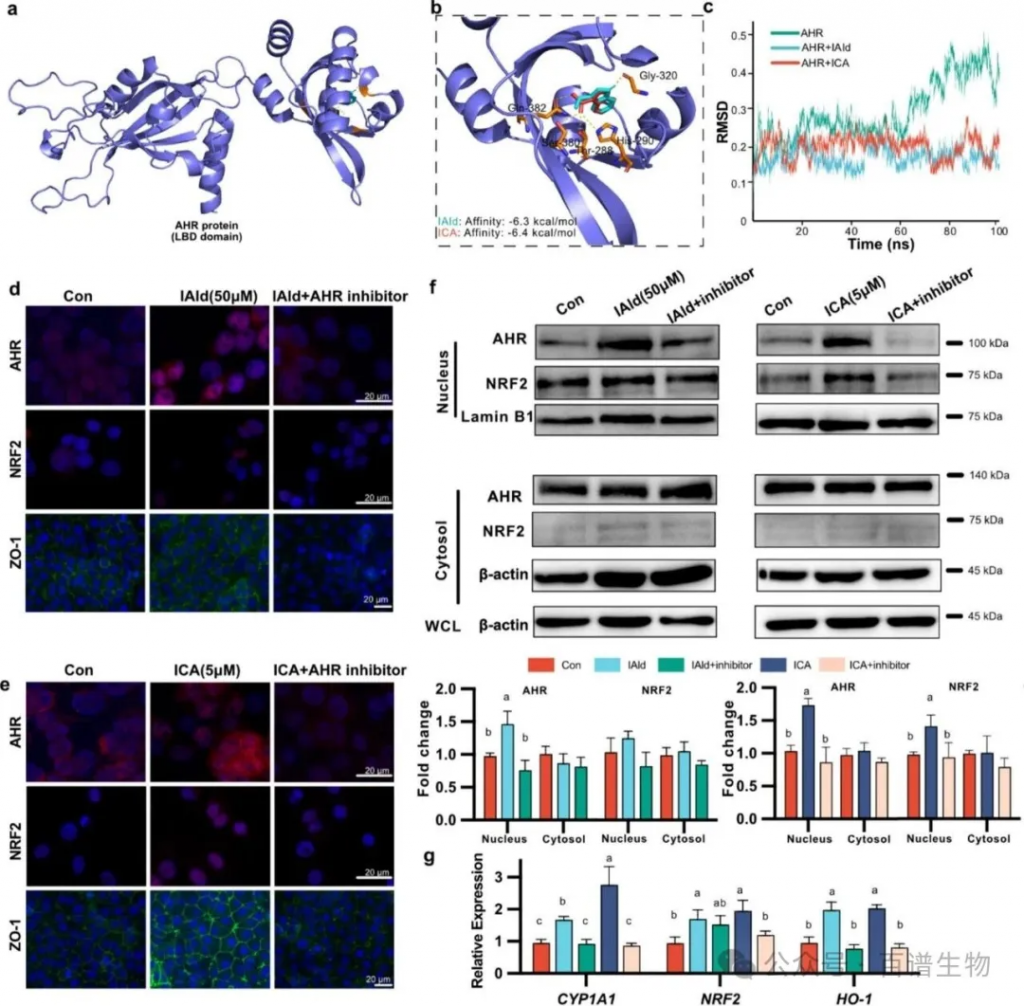
图6 探讨IAld与ICA促进肠上皮屏障功能及减轻炎症与氧化的潜在机制
分子对接与MD模拟证实,IAld可与AHR蛋白形成3个氢键,ICA可形成4个氢键,且ICA-AHR复合物RMSD值<0.2nm,结合更稳定。细胞试验显示,IAld/ICA 处理可促进AHR从细胞质向细胞核转位,显著上调下游CYP1A1、NRF2、HO-1基因表达;WB证实NRF2核蛋白表达水平在ICA处理组显著升高。AHR抑制剂可逆转上述调控效应,证实IAld/ICA通过激活AHR–NRF2通路,上调紧密连接蛋白表达并增强抗氧化能力,为其肠道保护作用的核心机制。
总结与讨论
综上,本方案以顶刊文献为支撑,融合多组学技术、覆盖多畜禽物种,既可为科研项目提供严谨设计框架,也能为养殖行业肠道健康监测提供落地工具,助力畜牧业精准防控肠源性疾病、推进减抗替抗进程。



