IF=14.1!浙大一附院团队新发现拿下高分一区TOP,代谢组+机器学习看清消化道疾病的4类风险人群

项目文章 | 帕金森病治疗添新招!广州医科大学团队揭秘RRx-001的“中枢+肠脑轴”调控机制
2026 年 2 月 11 日
桃果研究里程碑!全新调控模块揭秘,谷氨酸竟成风味与抗病性双优关键
2026 年 3 月 9 日
近日,浙江大学医学院附属第一医院团队在国际知名期刊Advanced Science(IF=14.1)发表最新研究成果,题为Integrated Metabolic and Inflammatory Clustering Reveals Distinct Risk Profiles for Digestive Diseases。研究基于英国生物银行39万余人的超大样本,首次构建了整合代谢与炎症的聚类分析框架,划分出四种代谢-炎症亚型,结合转录组、代谢组及机器学习技术,揭示了不同亚型与消化道疾病的风险关联及核心调控机制,为消化道疾病的精准风险评估、早期筛查和靶向干预提供了全新的理论依据与临床工具。

文章题目:Integrated Metabolic and Inflammatory Clustering Reveals Distinct Risk Profiles for Digestive Diseases
期刊名称:Advanced Science
影响因子:14.1
发表时间:2025年9月
研究方法:代谢组+机器学习
研究思路:
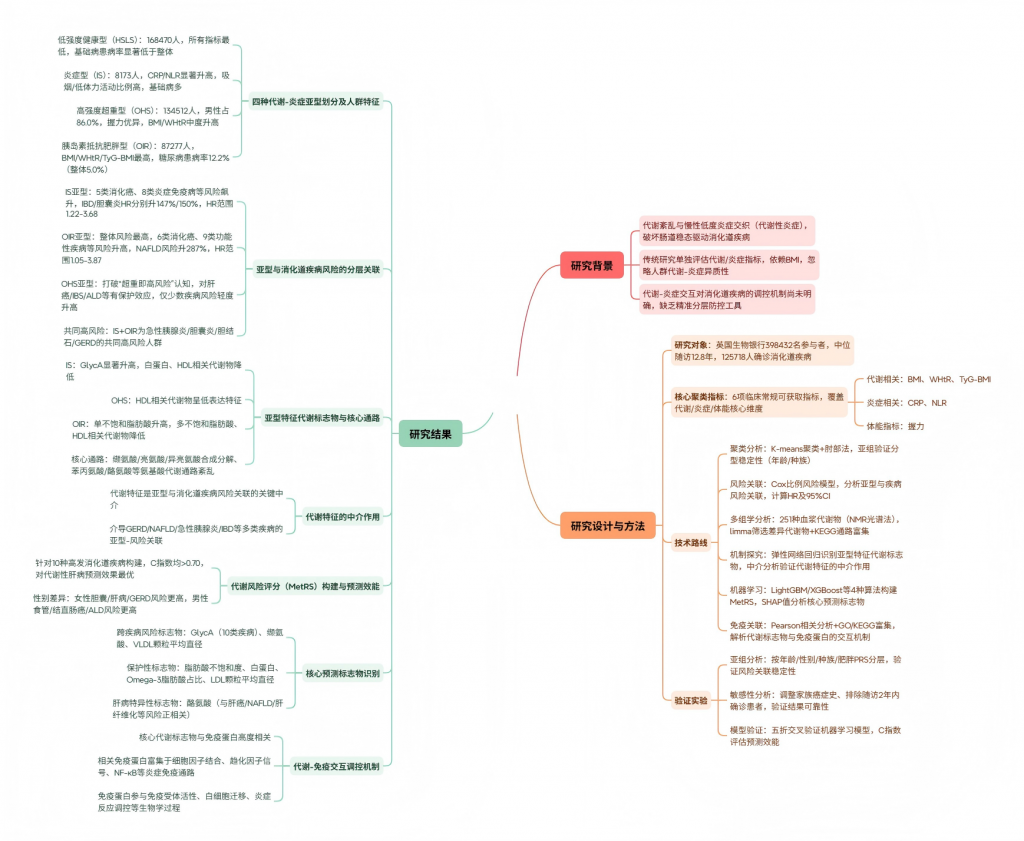
材料方法


主要结果
该研究以英国生物银行398432名参与者为对象,经K-means聚类分析将研究人群划分为低强度健康型(HSLS)、炎症型(IS)、高强度超重型(OHS)、胰岛素抵抗肥胖型(OIR)四种代谢-炎症亚型,且该分型在不同年龄、种族亚组中稳定性良好。中位12.8年的随访显示,IS亚型多种消化癌、炎症免疫病等风险显著升高,OIR亚型为消化道疾病整体最高风险亚型,NAFLD等代谢性肝病风险尤为突出,二者还是急性胰腺炎、胆囊炎等疾病的共同高风险人群,而OHS亚型打破传统认知,对肝癌、IBS等多种疾病呈现保护效应。代谢组学分析发现各亚型存在特征性差异代谢物,核心代谢差异集中在缬氨酸、亮氨酸等氨基酸合成与分解通路,且代谢特征是介导亚型与消化道疾病风险关联的关键环节。基于251种血浆代谢物结合机器学习构建的疾病特异性代谢风险评分,对10种高发消化道疾病预测C指数均超0.70,其中糖蛋白乙酰化产物(GlycA)、缬氨酸、酪氨酸、脂肪酸不饱和度为核心预测标志物,GlycA更是在10类疾病中表现出强预测能力。此外,核心代谢标志物与免疫蛋白高度相关,相关免疫蛋白富集于细胞因子结合、NF-κB信号等炎症免疫通路,证实代谢-免疫交互作用是调控消化道疾病发生的重要机制,同时亚组和敏感性分析也验证了各亚型与消化道疾病风险关联的稳健性。
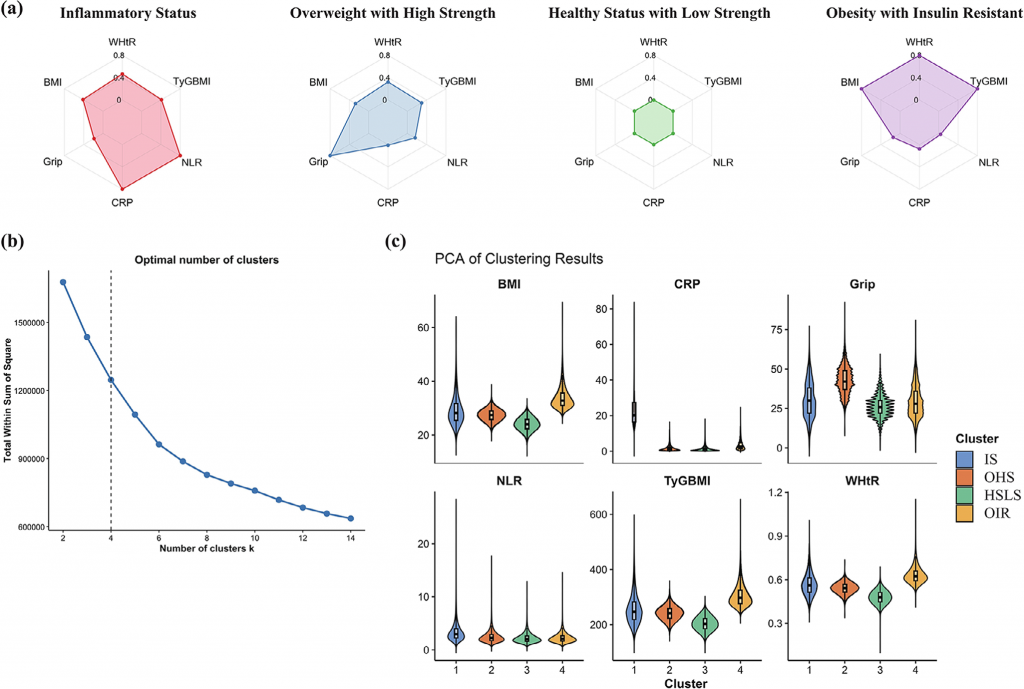
图1 队列研究中不同聚类的比例及特征
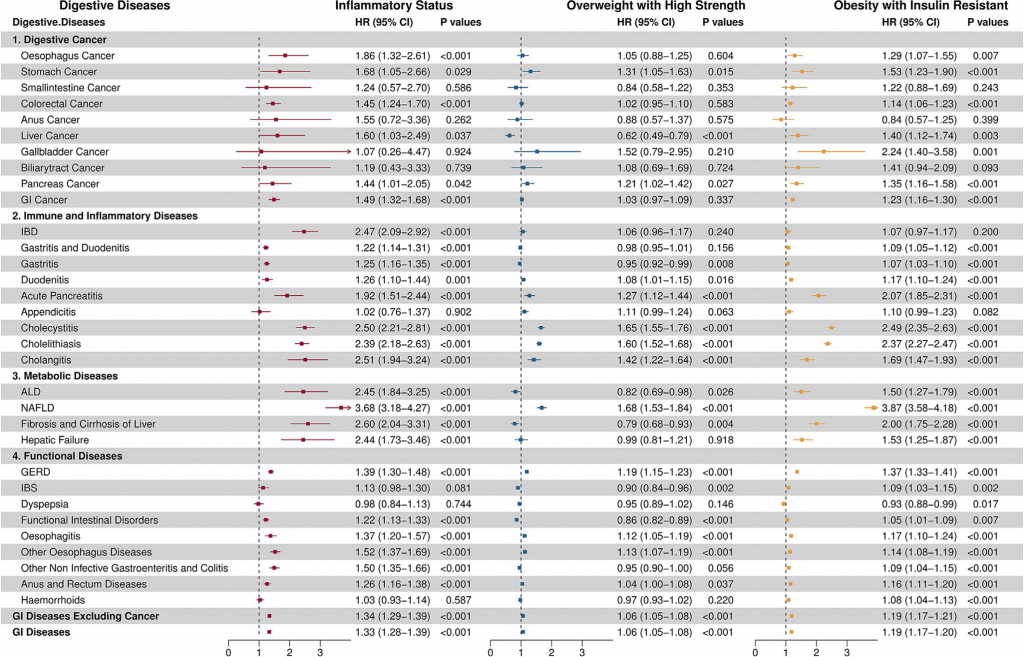
图2 人体测量学集群与消化系统疾病风险关联的Cox分析
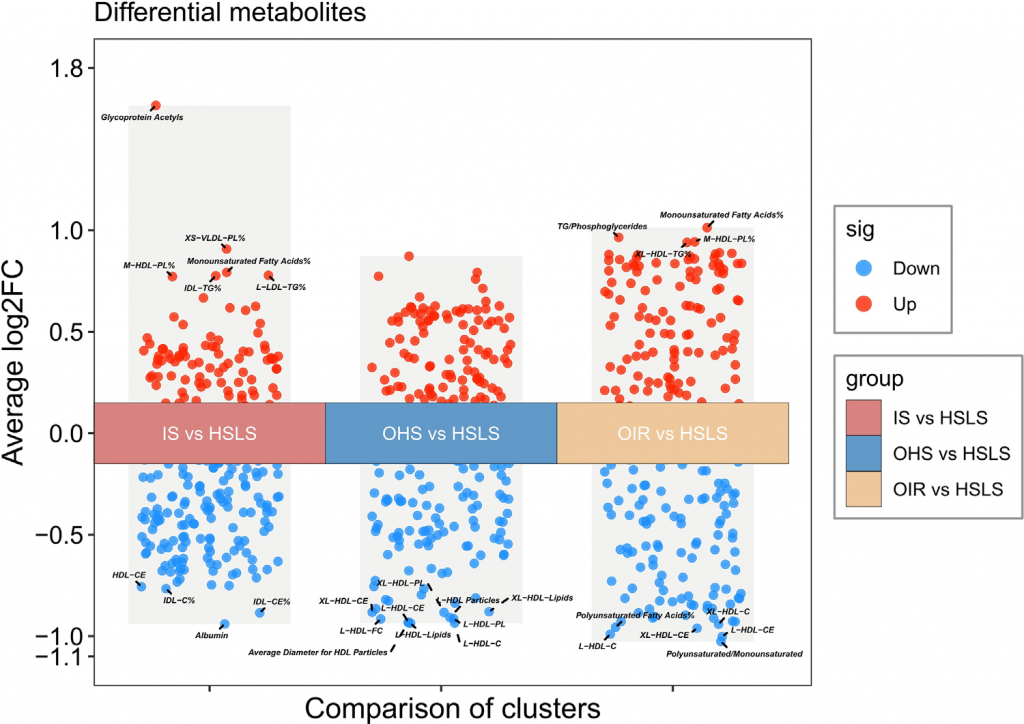
图3 展示各簇间差异代谢物的火山图
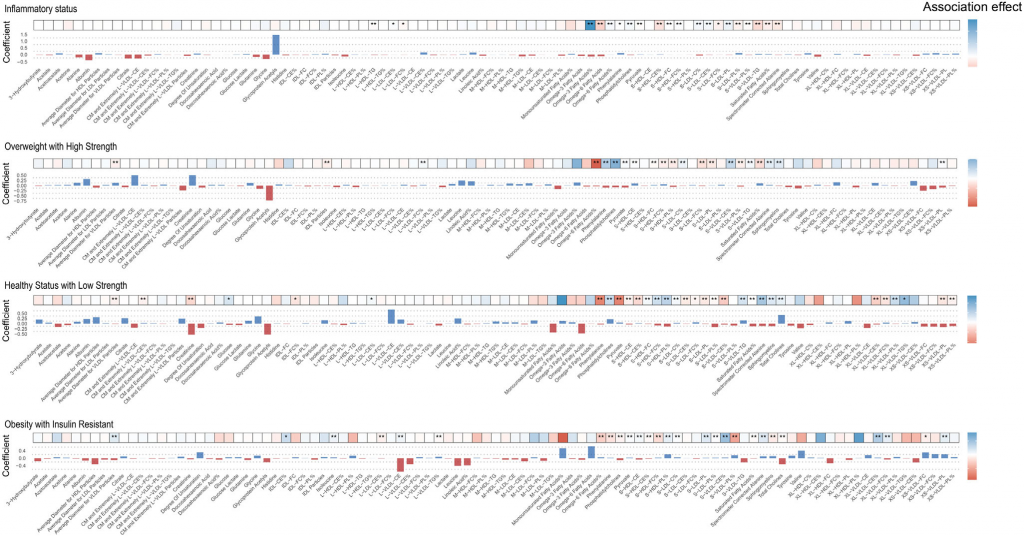
图4 代谢特征中选定代谢物与四个聚类的关联性分析
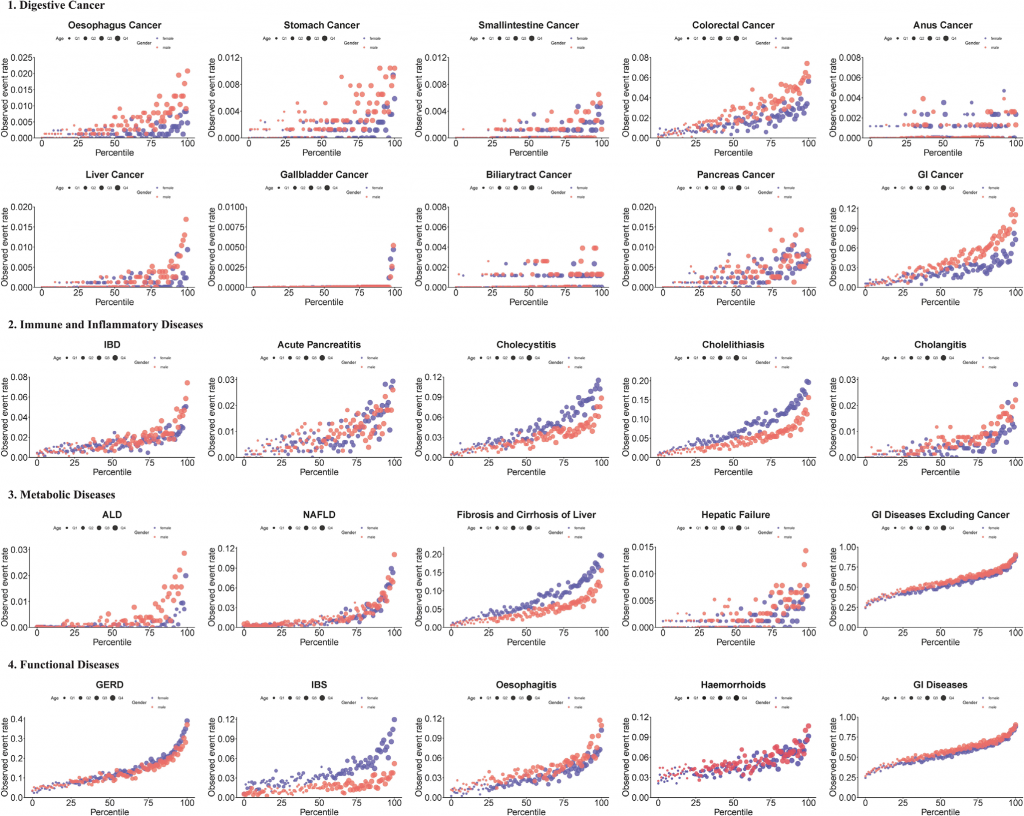
图5 25种新发疾病类别的观察事件频率与最佳模型百分位数的对应关系
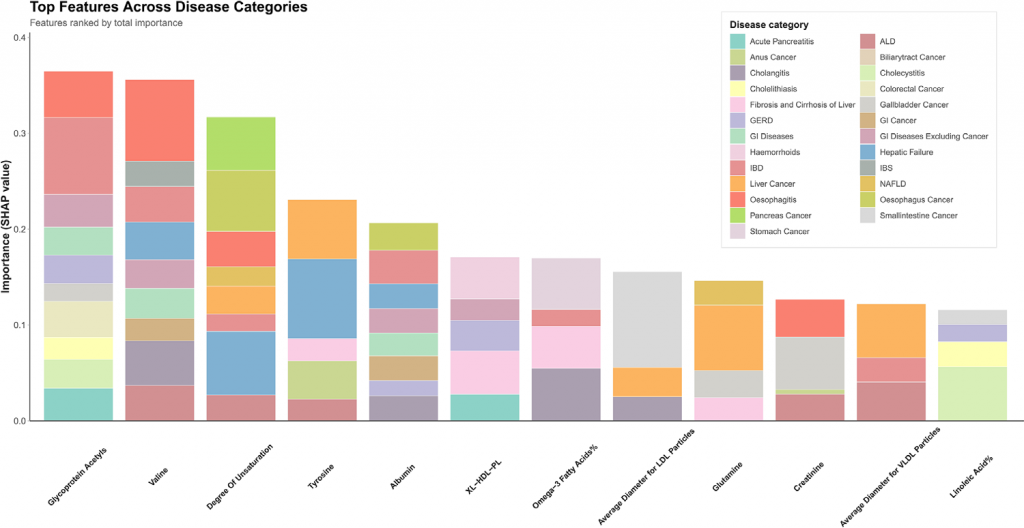
图6 25种疾病类别中机器学习模型标准化Shap值的堆叠条形图
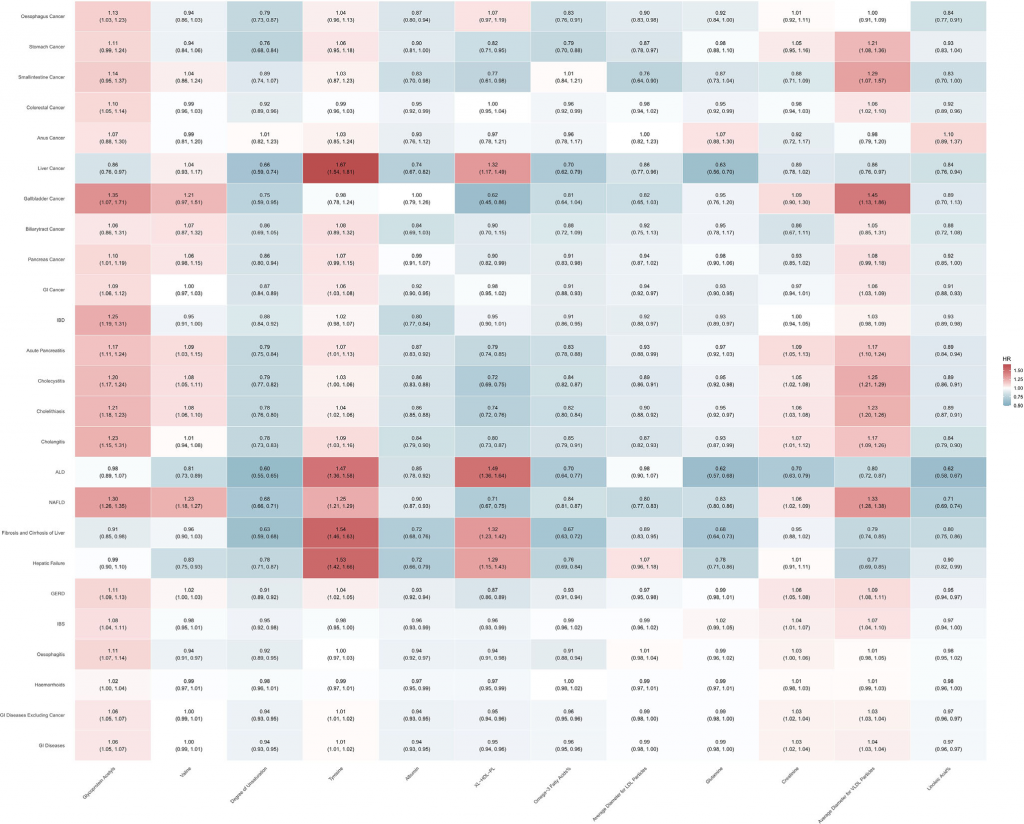
图7 图6所示代谢物与25项结局指标的关联性分析




